اللوكيميا (ابيضاض الدم): الأعراض والأسباب وخيارات العلاج الحديثة المتوفرة
كيف تطورت نسب الشفاء من سرطان الدم وما الخيارات العلاجية المتاحة اليوم؟
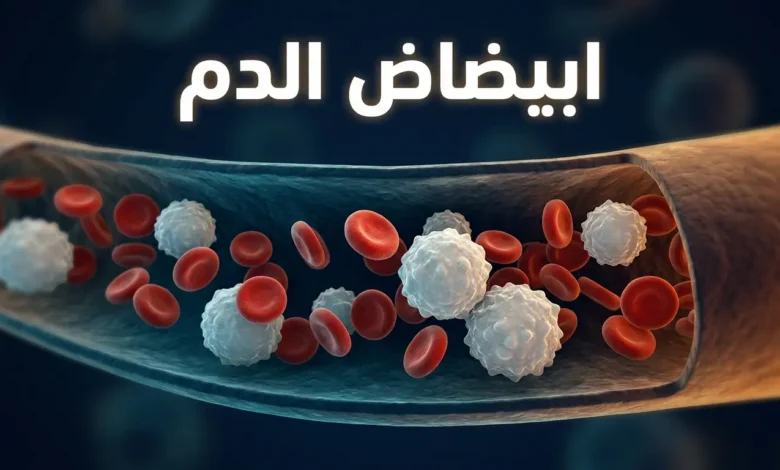
اللوكيميا — أو ابيضاض الدم — سرطان يبدأ في نخاع العظم ويُصيب خلايا الدم البيضاء، فيدفعها إلى التكاثر على نحو غير منضبط. تشمل أنواعها الحادة والمزمنة، الليمفاوية والنقوية. تُقدَّر الإصابات الجديدة عالمياً بنحو 487,000 حالة سنوياً وفق الوكالة الدولية لأبحاث السرطان. لقد تجاوزت نسب الشفاء في بعض الأنواع 90% عند الأطفال بفضل العلاجات الموجّهة والمناعية.
د. مها منصور — اختصاصية الأورام والطب النووي
د. سوزان عبد الحميد السعدي — استشارية أمراض الدم وزرع الخلايا الجذعية
تنبيه: المعلومات الواردة في هذا المقال هي للتثقيف الصحي فقط ولا تغني بأي حال عن استشارة الطبيب المختص.
أهم ما يجب أن تعرفه في أقل من دقيقة
🎯 حقائق علمية جوهرية
- اللوكيميا سرطان يبدأ في نخاع العظم ويُصيب خلايا الدم البيضاء — لا يُشكّل ورماً صلباً.
- 4 أنواع رئيسية: ALL وAML (حادة — تتطور بأيام) وCLL وCML (مزمنة — تتطور ببطء).
- نسبة الشفاء التام من ALL عند الأطفال تجاوزت 90% في المراكز المتقدمة.
- كروموسوم فيلادلفيا في CML أدى إلى تطوير دواء إيماتينيب الذي حوّل المرض إلى حالة مزمنة يمكن التعايش معها.
🚨 علامات تستدعي الطبيب فوراً
- حمى مستمرة أكثر من أسبوع لا تستجيب للمسكّنات.
- كدمات واسعة دون إصابة واضحة أو نزيف لا يتوقف.
- إنهاك شديد مع شحوب مفاجئ وضيق تنفس.
- تضخم عقد لمفاوية لم يختفِ خلال 2-3 أسابيع.
💊 خيارات العلاج المتاحة اليوم
- كيميائي: حجر الأساس في اللوكيميا الحادة — بروتوكولات محددة لكل نوع.
- موجّه: أدوية تستهدف الطفرة الجينية بدقة مثل إيماتينيب وفينيتوكلاكس.
- مناعي (CAR-T): خلايا مناعية مُعدَّلة جينياً لمهاجمة الخلايا السرطانية.
- زراعة خلايا جذعية: للحالات عالية الخطورة أو المنتكسة.
✅ خطوتك الآن
- اطلب تحليل دم شاملاً (CBC) إذا لاحظت أياً من الأعراض المذكورة.
- لا تتأخر عن الطبيب — الكشف المبكر يُضاعف فرص الشفاء.
- لا تعتمد على الأعشاب أو المكملات بديلاً عن العلاج الطبي.
هل تلقيت يوماً خبراً عن إصابة قريب أو صديق بسرطان الدم فشعرت أن الأرض تميد تحت قدميك؟ ربما سمعت كلمة “لوكيميا” فتخيّلت أنها حكم نهائي لا رجعة فيه. أنت لست وحدك في هذا الشعور، لكنّ الحقيقة مختلفة تماماً عمّا يرسمه الخوف. في هذا المقال ستفهم المرض من جذوره، وستعرف كيف أصبح الطب الحديث قادراً على مواجهته بأدوات لم تكن موجودة قبل عقد واحد. المعرفة هنا ليست ترفاً؛ إنها أول خطوة نحو قرار صحيح وهدوء نفسي حقيقي.
تخيّل أن “سارة”، أمّ لطفلين في الرياض، لاحظت أن ابنها أحمد (6 سنوات) يعاني من إرهاق غير مبرر وكدمات تظهر على ذراعيه دون سبب واضح. ذهبت به إلى طبيب الأطفال الذي طلب تحليل دم شاملاً. أظهرت النتائج ارتفاعاً غير طبيعي في خلايا الدم البيضاء مع انخفاض الصفائح الدموية. أُحيل أحمد فوراً إلى اختصاصي أمراض الدم، وبعد خزعة نخاع العظم جاء التشخيص: ابيضاض الدم الليمفاوي الحاد (ALL). بدأت سارة تشعر بالذعر، لكن الطبيب أخبرها بأن نسبة الشفاء التام لهذا النوع عند الأطفال تتجاوز 90%. بدأ أحمد بروتوكول العلاج الكيميائي، وبعد أشهر من المتابعة الدقيقة دخل مرحلة الهدأة الكاملة (Complete Remission). الخلاصة: الكشف المبكر والالتزام بالبروتوكول العلاجي يصنعان فارقاً هائلاً.
ما هي اللوكيميا علمياً وكيف تختلف عن الأورام الصلبة؟
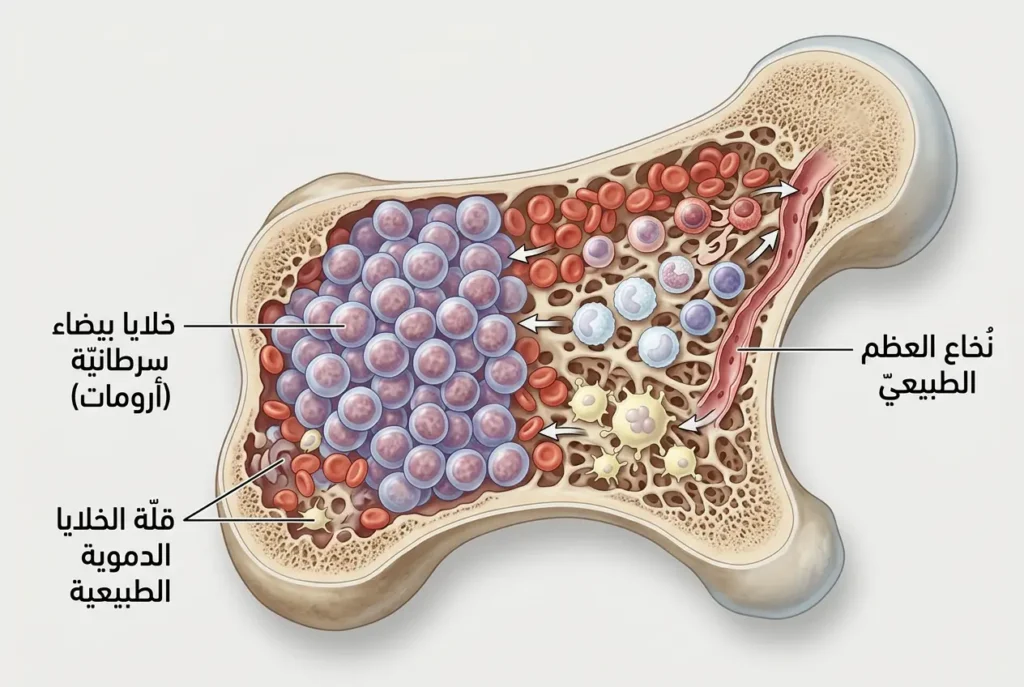
لكي تفهم سرطان الدم، عليك أن تتخيّل نخاع العظم كمصنع ضخم يعمل على مدار الساعة. هذا المصنع — المختبئ داخل عظامك الكبيرة كعظم الحوض والفخذ والقص — ينتج يومياً مليارات الخلايا الدموية الجديدة. ثلاثة خطوط إنتاج تعمل في وقت واحد: خط كريات الدم الحمراء (Red Blood Cells) التي تنقل الأكسجين إلى كل خلية في جسمك، وخط كريات الدم البيضاء (White Blood Cells) التي تُشكّل جيش المناعة، وخط الصفائح الدموية (Platelets) التي تُرقّع أي جرح وتوقف النزيف.
في الوضع الطبيعي، تنضج كل خلية وتخرج من المصنع جاهزة لأداء وظيفتها ثم تموت بعد عمرها الافتراضي — وهذا ما يُسمّى الموت الخلوي المبرمج (Apoptosis). لكن في اللوكيميا يحدث عطل جوهري في خط الإنتاج: تبدأ خلايا بيضاء غير ناضجة بالتكاثر على نحو جنوني دون أن تنضج ودون أن تموت في موعدها. تخيّل أن خط إنتاج الجنود في المصنع يُصدر آلاف الجنود غير المدرّبين الذين يحتلون المصنع ويمنعون الخطوط الأخرى من العمل. النتيجة: ينخفض إنتاج كريات الدم الحمراء فيظهر فقر الدم (Anemia)، وتقلّ الصفائح الدموية فتحدث النزوف والكدمات، وتتراكم الخلايا البيضاء غير الوظيفية فيضعف الجهاز المناعي رغم ارتفاع عددها الظاهري.
الفارق الجوهري بين اللوكيميا والأورام الصلبة — كسرطان الرئة أو الثدي مثلاً — هو أن اللوكيميا لا تُشكّل كتلة يمكن استئصالها جراحياً. إنها منتشرة في الدم ونخاع العظم منذ البداية، وهذا ما جعل علاجها يعتمد على أساليب جهازية (Systemic Therapies) تصل إلى كل ركن في الجسم.
حقيقة طبية: نخاع العظم لدى الإنسان البالغ يُنتج ما يقارب 200 مليار كرية دم حمراء و10 مليارات كرية بيضاء يومياً. أي خلل في هذا المعدل الهائل يمكن أن يُحدث اضطراباً سريعاً في وظائف الجسم كلها.
اقرأ أيضاً:
لماذا يحدث الخطأ الجيني الذي يُشعل اللوكيميا؟
ما الذي يجعل خلية طبيعية في نخاع العظم تتحوّل فجأة إلى خلية سرطانية؟ الإجابة تكمن في الطفرات الجينية (Genetic Mutations). كل خلية في جسمك تحتوي على شريط الحمض النووي (DNA) الذي يعمل كدليل تعليمات مفصّل. هذا الدليل يُحدّد متى تنقسم الخلية ومتى تنضج ومتى تتوقف عن الانقسام ومتى تموت.
في اللوكيميا، تُصاب جينات محدّدة بطفرات تُعطّل هذه التعليمات. بعض هذه الطفرات تُنشّط ما يُسمّى الجينات الورمية (Oncogenes) — وكأنك ضغطت على دوّاسة البنزين في سيارة ولم ترفع قدمك. وبعضها الآخر يُعطّل الجينات الكابتة للورم (Tumor Suppressor Genes) — وكأنك قطعت كوابح السيارة. الجمع بين التسارع وفقدان الكبح يُنتج انقساماً خلوياً جنونياً لا يتوقف.
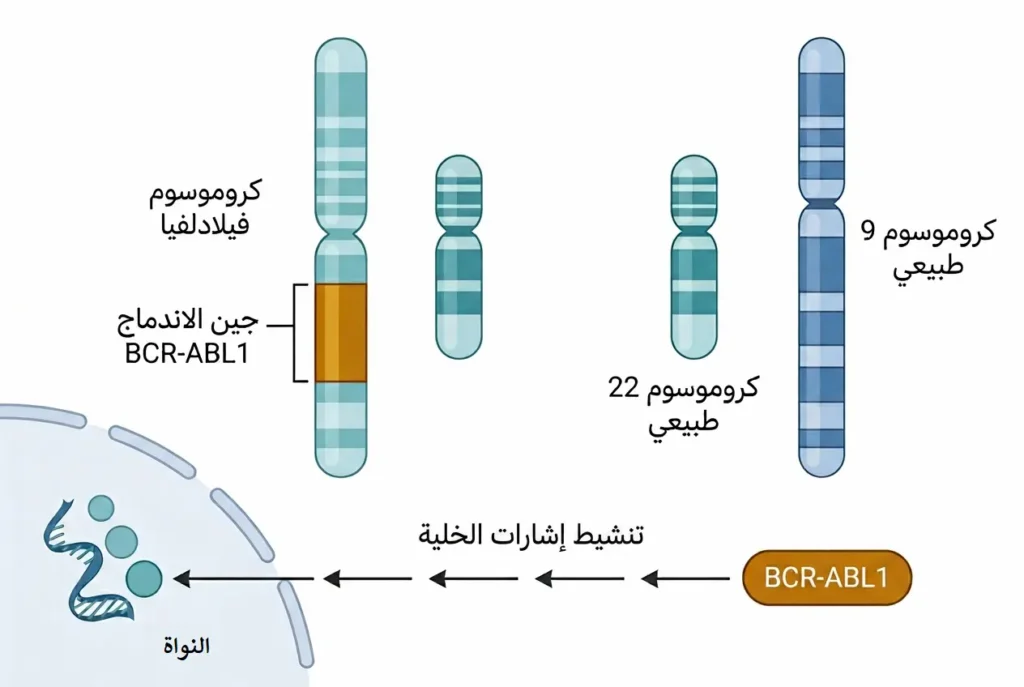
من أشهر الأمثلة على ذلك كروموسوم فيلادلفيا (Philadelphia Chromosome) الذي يظهر في معظم حالات ابيضاض الدم النقوي المزمن (CML). هنا يحدث تبادل غير طبيعي بين أجزاء من الكروموسوم 9 والكروموسوم 22، فينتج جين اندماجي يُسمّى BCR-ABL1 يُنتج بروتيناً يُحفّز الخلايا على الانقسام باستمرار. هذا الاكتشاف لم يكن مجرد معلومة أكاديمية؛ بل أدّى إلى تطوير دواء إيماتينيب (Imatinib) — المعروف تجارياً بـ غليفيك (Gleevec) — الذي حوّل سرطان الدم النقوي المزمن من مرض قاتل إلى حالة مزمنة يمكن التعايش معها لعقود.
لكن انتبه: ليس كل من يحمل طفرة جينية مُعرّضاً يُصاب حتماً باللوكيميا. معظم الطفرات تحتاج إلى عوامل مُساعدة — كالتعرض المتكرر لمواد كيميائية معينة أو الإشعاع أو حتى الصدفة البيولوجية — لكي تتحوّل إلى مرض فعلي. وهذا ما يفسّر لماذا يُصاب شخص دون آخر رغم تشابه ظروفهما.
اقرأ أيضاً:
كم نوعاً للوكيميا ولماذا يُعَدّ التصنيف مفتاحاً للعلاج؟
تصنيف اللوكيميا ليس مجرد تمرين أكاديمي؛ بل هو الخطوة الأولى التي يبني عليها الطبيب خطته العلاجية بالكامل. فكل نوع يختلف في سلوكه وسرعته واستجابته للأدوية. فما هي الأنواع الرئيسة يا ترى؟
ابيضاض الدم الليمفاوي الحاد (Acute Lymphoblastic Leukemia — ALL)
هذا النوع هو الأكثر شيوعاً بين الأطفال، ويبلغ ذروته بين سن 2 و5 سنوات. يبدأ في الخلايا الليمفاوية غير الناضجة (Lymphoblasts) ويتطور بسرعة كبيرة. الخبر المفرح — وأقولها بثقة — أن نسبة الشفاء التام من ابيضاض الدم الليمفاوي الحاد عند الأطفال تجاوزت 90% في المراكز المتقدمة، وفقاً لبيانات الجمعية الأميركية للسرطان. لقد تحوّل هذا المرض من كابوس إلى قصة نجاح طبية حقيقية.
ابيضاض الدم النقوي الحاد (Acute Myeloid Leukemia — AML)
يُصيب الخلايا النقوية (Myeloid Cells) وهو أكثر شيوعاً عند البالغين وكبار السن. يتميز بسرعة تطوره أيضاً، لكن بروتوكولات العلاج تطوّرت بشكل ملحوظ في السنوات الأخيرة. فقد وافقت إدارة الغذاء والدواء الأميركية (FDA) بين عامي 2017 و2024 على أكثر من 10 أدوية جديدة موجّهة لعلاج أنواع فرعية محدّدة من هذا السرطان.
ابيضاض الدم الليمفاوي المزمن (Chronic Lymphocytic Leukemia — CLL)
هو النوع الأكثر شيوعاً بين البالغين في الدول الغربية. يتطور ببطء شديد، وكثير من المرضى لا يحتاجون إلى علاج فوري عند التشخيص؛ بل يُراقَبون فقط — وهذا ما يُسمّى إستراتيجية “المراقبة والانتظار” (Watch and Wait). قد يعيش المريض سنوات طويلة دون أعراض.
ابيضاض الدم النقوي المزمن (Chronic Myeloid Leukemia — CML)
هذا هو النوع الذي أحدث ثورة في مفهوم العلاج الموجّه. بفضل مثبطات التيروزين كيناز (Tyrosine Kinase Inhibitors — TKIs) مثل إيماتينيب ونيلوتينيب (Nilotinib) وداساتينيب (Dasatinib)، أصبح معدل البقاء على قيد الحياة لعشر سنوات يتجاوز 85%.
| وجه المقارنة | ALL ليمفاوي حاد |
AML نقوي حاد |
CLL ليمفاوي مزمن |
CML نقوي مزمن |
|---|---|---|---|---|
| الفئة الأكثر إصابةً | الأطفال (2-5 سنوات) | البالغون وكبار السن | فوق 60 عاماً | البالغون (30-60 عاماً) |
| سرعة التطور | سريع جداً | سريع جداً | بطيء جداً | بطيء إلى متوسط |
| العلاج الرئيسي | كيميائي + مناعي | كيميائي + موجّه | مراقبة أو مثبطات BTK | مثبطات TKI (فموي) |
| نسبة البقاء 5 سنوات | >90% (أطفال) | 25-30% (عموماً) | >85% | >85% (10 سنوات) |
| طفرة جينية مميّزة | إعادة ترتيب MLL | FLT3 / NPM1 / IDH1-2 | حذف 17p / طفرة TP53 | BCR-ABL1 (كروموسوم فيلادلفيا) |
| الحاجة لزراعة خلايا | في الحالات عالية الخطورة | شائعة في مرحلة الهدأة | نادرة | عند مقاومة TKI |
رقم لافت: في ثمانينيات القرن الماضي كان متوسط البقاء بعد تشخيص CML يتراوح بين 3 و5 سنوات فقط. اليوم، ومع العلاجات الموجّهة، أصبح كثير من المرضى يعيشون عمراً طبيعياً تقريباً — وهذا تحوّل جذري لا مثيل له في تاريخ الطب.
الفرق الجوهري بين اللوكيميا الحادة والمزمنة
السؤال الذي يطرحه كثير من المرضى: ما الفرق بين اللوكيميا الحادة والمزمنة؟ الجواب ببساطة يتعلّق بسرعة تطور المرض ونضج الخلايا. في الحادة، تتكاثر خلايا غير ناضجة تماماً (أرومات — Blasts) بسرعة هائلة وتحتاج إلى علاج فوري خلال أيام. أما في المزمنة، فالخلايا تكون أكثر نضجاً نسبياً وتتراكم ببطء على مدى أشهر أو سنوات. لا يعني “مزمنة” أنها أخف خطورة بالضرورة، لكنها تمنح الأطباء وقتاً أكبر للتخطيط العلاجي.
| وجه المقارنة | اللوكيميا الحادة (ALL / AML) |
اللوكيميا المزمنة (CLL / CML) |
|---|---|---|
| نضج الخلايا | خلايا غير ناضجة تماماً (أرومات) | خلايا أكثر نضجاً نسبياً |
| سرعة التطور | أيام إلى أسابيع — حرجة | أشهر إلى سنوات — تدريجية |
| الحاجة للعلاج الفوري | ضرورة قصوى — فوري | قد يُؤجَّل (Watch & Wait) |
| الأعراض عند التشخيص | حادة وواضحة في الغالب | قد تكون صامتة أو خفيفة |
| كثافة العلاج | عالية جداً — كيميائي مكثف | معتدلة — فموي في الغالب |
| احتمالية الشفاء التام | مرتفعة (خاصة ALL الأطفال) | عادةً تحكّم طويل الأمد لا شفاء تام |
| نسبة الأرومات في النخاع | ≥20% — معيار التشخيص | <20% — تراكم تدريجي |
| إمكانية التوقف عن العلاج | بعد الشفاء التام فقط | في CML: TFR ممكنة تحت إشراف |
ما الذي يجعل اللوكيميا تختلف عن كل السرطانات الأخرى في آليتها الخلوية؟
هذه الفقرة هي النقطة التي ستفهم فيها لماذا يتصرف سرطان الدم بهذا الشكل الفريد. في معظم السرطانات الصلبة، تبدأ خلية واحدة في عضو محدّد بالانقسام وتُشكّل كتلة ورمية (Tumor Mass) يمكن رؤيتها بالتصوير واستئصالها جراحياً. لكن في اللوكيميا، الخلايا السرطانية موجودة في نسيج سائل — الدم ونخاع العظم — وهذا يعني أنها منتشرة في كل أنحاء الجسم من لحظة نشأتها.
هذا الانتشار الأوّلي الذي يُخيف الناس هو في الواقع ما جعل العلاج الجهازي (الكيميائي والموجّه والمناعي) فعّالاً للغاية؛ لأن الأدوية التي تسري في مجرى الدم تصل مباشرة إلى الخلايا السرطانية أينما كانت. لا حاجة لجراحة معقدة ولا لتحديد موقع ورم محدّد. إنها مفارقة رائعة: الخاصية التي تبدو مخيفة — الانتشار — هي نفسها التي تجعل العلاج أسهل وصولاً.
من ناحية أخرى، تمتلك خلايا اللوكيميا ميزة خبيثة: قدرتها على الاختباء في ما يُسمّى “الملاذات المحمية” (Sanctuary Sites) مثل الجهاز العصبي المركزي والخصيتين، إذ لا تصل بعض الأدوية بسهولة إلى هذه المناطق بسبب الحاجز الدموي الدماغي (Blood-Brain Barrier). ولهذا السبب تتضمّن بعض بروتوكولات العلاج حقناً مباشراً في السائل الشوكي — يُسمّى العلاج داخل القراب (Intrathecal Therapy) — لملاحقة أي خلية سرطانية اختبأت هناك.
المختبر الفسيولوجي — للمهتمين بالتفاصيل العلمية الدقيقة
على المستوى الجزيئي، تنطلق اللوكيميا من خلل في مسارات الإشارات الخلوية (Cell Signaling Pathways) التي تتحكم في دورة حياة الخلية الجذعية المكوّنة للدم (Hematopoietic Stem Cell — HSC). في الأحوال الطبيعية، تخضع هذه الخلايا لتنظيم دقيق من خلال عدة مسارات متداخلة، أبرزها مسار JAK-STAT ومسار RAS-MAPK ومسار PI3K-AKT-mTOR. كل مسار من هذه المسارات يعمل كصمام تنظيمي: يسمح بالانقسام عند الحاجة ويُوقفه عند الاكتفاء.
في ابيضاض الدم النقوي الحاد (AML)، تُحدث طفرات في جين FLT3 (Fms-Like Tyrosine Kinase 3) تنشيطاً مستمراً لمسار RAS-MAPK، مما يُبقي الخلية في حالة انقسام دائم. هذا الجين يُشفّر مستقبلاً من نوع تيروزين كيناز يقع على سطح الخلية الجذعية المكوّنة للدم. عندما يتحوّر هذا المستقبل، يبقى نشطاً حتى في غياب الإشارة الطبيعية (اللجين — Ligand) التي تُنشّطه — وكأن مفتاح الإضاءة عالق في وضع التشغيل ولا يمكن إطفاؤه.
في ابيضاض الدم النقوي المزمن (CML)، يُنتج الجين الاندماجي BCR-ABL1 بروتيناً شاذاً بنشاط تيروزين كيناز مستمر. هذا البروتين يُفعّل عدة مسارات في وقت واحد: يُعزّز الانقسام عبر RAS-MAPK، ويمنع الموت الخلوي المبرمج عبر تثبيط بروتين BAX (المُحفّز لإطلاق السيتوكروم C من الميتوكوندريا)، ويُنشّط STAT5 الذي يُعزّز بقاء الخلية. فهم هذه الآلية هو بالضبط ما أدّى إلى تصميم مثبطات التيروزين كيناز التي تسدّ الموقع النشط للبروتين الشاذ وتُوقف كل هذه المسارات دفعة واحدة.
أما في ابيضاض الدم الليمفاوي الحاد (ALL)، فتلعب إعادة ترتيب جين MLL (Mixed Lineage Leukemia) دوراً محورياً في كثير من الحالات عند الرضّع. هذا الجين يُشفّر بروتيناً يعمل كمنظّم فوقجيني (Epigenetic Regulator) يتحكم في تشغيل جينات أخرى عبر تعديل بنية الهستونات (Histone Methylation). عندما ينكسر هذا الجين ويلتحم مع شريك اندماجي، يفقد الخلية الليمفاوية قدرتها على النضج وتبقى عالقة في مرحلة الأرومة.
الجدير بالذكر أن مفهوم “البيئة المكروية لنخاع العظم” (Bone Marrow Microenvironment) أصبح محوراً بحثياً مهماً. فالخلايا السرطانية لا تعيش بمعزل؛ بل تتواصل مع الخلايا اللحمية (Stromal Cells) والخلايا البطانية الوعائية عبر إشارات كيميائية مثل CXCL12 ومستقبله CXCR4. هذا التواصل يُوفّر للخلايا السرطانية حماية من العلاج الكيميائي، ولهذا السبب تُجرى حالياً تجارب سريرية على أدوية تستهدف هذا المحور لكسر الحماية وجعل الخلايا أكثر عُرضة للأدوية.
ما أعراض اللوكيميا التي يجب ألا تتجاهلها أبداً؟
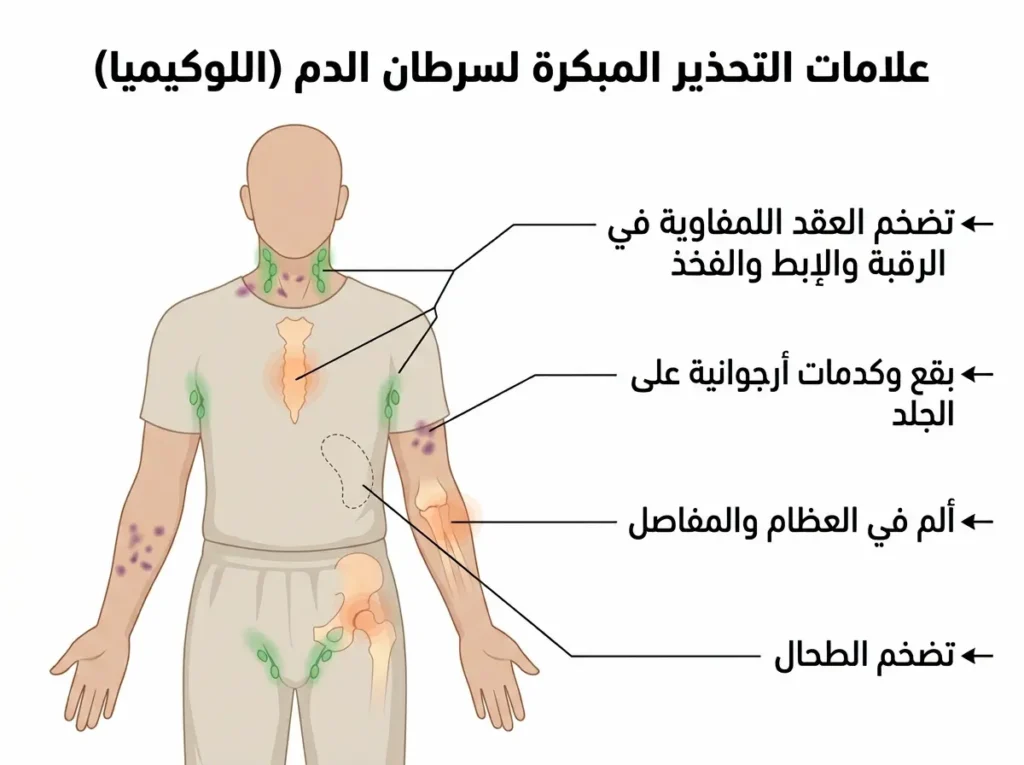
أعراض ابيضاض الدم قد تبدو في البداية عادية ومشابهة لحالات شائعة كالإنفلونزا أو الإرهاق المزمن. وهذا بالتحديد ما يجعل الانتباه لها مهماً للغاية؛ إذ إنّ الكشف المبكر يُضاعف فرص الشفاء. فلنمشِ معاً عبر أعراض ابيضاض الدم المبكرة والمتقدمة.
التعب والإنهاك المستمر هو عادةً أول ما يلاحظه المريض. ليس التعب العادي بعد يوم عمل طويل، بل إنهاك يجعلك تشعر أنك لا تستطيع النهوض من الفراش رغم نومك ساعات كافية. السبب هو نقص كريات الدم الحمراء السليمة التي تحمل الأكسجين إلى عضلاتك وأعضائك. كذلك ترتفع درجة الحرارة دون سبب واضح — حمّى متكررة أو مستمرة — لأن الجهاز المناعي مشغول بخلايا بيضاء غير وظيفية لا تستطيع مكافحة العدوى فعلياً. التعرق الليلي الغزير الذي يُبلل الملابس والوسادة هو عرض آخر يُقلق الأطباء فوراً.
من جهة ثانية، يُلاحظ كثير من المرضى ظهور كدمات على الجلد دون تعرّض لإصابة واضحة، أو نزيف من اللثة أو الأنف يصعب إيقافه. السبب واضح فسيولوجياً: الخلايا السرطانية تزاحم الصفائح الدموية في نخاع العظم فينخفض إنتاجها وتضعف قدرة الدم على التخثر. كما أن العدوى المتكررة — التهاب الحلق الذي لا يشفى، أو الالتهابات الجلدية المتكررة — تدلّ على خلل وظيفي في المناعة.
أما الأعراض المتقدمة فتشمل تضخم العقد اللمفاوية (Lymphadenopathy) الذي يظهر ككتل غير مؤلمة في الرقبة أو تحت الإبط أو في المنطقة الأربية. وقد يشعر المريض بألم في العظام — خاصة في عظم القص والحوض — بسبب تمدّد نخاع العظم المملوء بالخلايا السرطانية. كذلك قد يتضخم الكبد أو الطحال (Hepatosplenomegaly) فيشعر المريض بامتلاء أو ألم في الجزء العلوي الأيسر من البطن.
نقطة تستحق الانتباه: عند الأطفال، قد يظهر ألم العظام على شكل عَرج غير مفسّر أو رفض للمشي أو اللعب. إذا رأيت طفلك يتجنّب الحركة فجأة دون إصابة واضحة، فهذا يستحق زيارة الطبيب فوراً. لا تنتظر.
متى يجب التوجه إلى الطبيب فوراً؟
بعض العلامات لا تقبل التأجيل مطلقاً. إذا لاحظت أياً مما يلي، فتوجّه إلى أقرب قسم طوارئ أو اختصاصي أمراض دم:
- حمّى مستمرة لأكثر من أسبوع لا تستجيب للمسكّنات العادية ولا يمكن تفسيرها بعدوى معروفة.
- نزيف لا يتوقف من أي مكان في الجسم — اللثة، الأنف، البول، البراز.
- ظهور كدمات واسعة ومتعددة على الجلد دون سبب.
- فقدان وزن غير مقصود بنسبة تزيد عن 10% من وزنك خلال 6 أشهر.
- تضخم عقد لمفاوية لا يختفي خلال 2-3 أسابيع.
- شحوب شديد مفاجئ مع ضيق تنفس عند أقل مجهود.
ماذا تفعل الآن؟ اطلب من طبيبك تحليل دم شاملاً (CBC) مع مسحة دم (Blood Smear). هذا التحليل البسيط والرخيص يمكنه أن يكشف خللاً واضحاً في أعداد خلايا الدم ويُعطي أول إنذار قوي.
اقرأ أيضاً:
من هو الأكثر عُرضة للإصابة بسرطان الدم ولماذا؟
هل اللوكيميا مرض وراثي؟ هذا سؤال يطرحه كثير من الأهالي القلقين، خاصة إذا أُصيب أحد أفراد العائلة. الإجابة المختصرة: اللوكيميا ليست وراثية بالمعنى التقليدي في معظم الحالات، لكن بعض العوامل الوراثية ترفع الاستعداد.
الأطفال المصابون بمتلازمة داون (Down Syndrome / Trisomy 21) لديهم احتمال أعلى بنحو 10 إلى 20 ضعفاً للإصابة بابيضاض الدم مقارنة بالأطفال الآخرين. كذلك هناك متلازمات وراثية نادرة مثل متلازمة لي-فراوميني (Li-Fraumeni Syndrome) ومتلازمة فانكوني (Fanconi Anemia) ترفع المخاطر. لكن الغالبية العظمى من حالات سرطان الدم تحدث عند أشخاص ليس لديهم تاريخ عائلي واضح.
التعرض المزمن لبعض المواد الكيميائية يُعَدُّ عامل خطر مثبتاً. البنزين (Benzene) — الموجود في بعض البيئات الصناعية ودخان السجائر — مرتبط ارتباطاً وثيقاً بابيضاض الدم النقوي الحاد. دراسة منشورة في مجلة The Lancet Oncology عام 2019 أكّدت أن التعرض المهني للبنزين يرفع خطر AML بمقدار 2 إلى 3 أضعاف. كما أن التعرض للإشعاع المؤيَّن بجرعات عالية — كما حدث مع الناجين من القنابل الذرية في اليابان — يرفع المخاطر بوضوح.
من التاريخ الطبي، يُعَدُّ الحصول على علاج كيميائي أو إشعاعي سابق لسرطان آخر عاملاً مهماً. هناك ما يُسمّى اللوكيميا الثانوية (Secondary Leukemia / Therapy-Related Leukemia) التي تظهر بعد سنوات من علاج ورم سابق. بعض أدوية العلاج الكيميائي — خاصة من فئة الألكيلات (Alkylating Agents) ومثبطات توبوإيزوميراز II (Topoisomerase II Inhibitors) — تحمل هذا الخطر.
ومضة علمية: التدخين يرفع خطر الإصابة بابيضاض الدم النقوي الحاد (AML) بنسبة 40% وفقاً لتحليل تجميعي (Meta-Analysis) نُشر في مجلة Blood عام 2020. لعل هذا الرقم يُضاف إلى قائمة الأسباب التي تدفعك — إن كنت مدخّناً — إلى اتخاذ قرار الإقلاع اليوم.
هل يمكن الوقاية من سرطان الدم بخطوات استباقية؟
لعل السؤال الذي يتبادر إلى ذهنك الآن: “إذا عرفنا عوامل الخطر، فهل يمكنني حماية نفسي وعائلتي من اللوكيميا؟” الإجابة الطبية المباشرة هي أنه لا توجد طريقة مؤكدة 100% للوقاية من معظم أنواع ابيضاض الدم، لأن الطفرات الجينية تحدث غالباً لأسباب لا نملك السيطرة الكاملة عليها. ومع ذلك، هناك تغييرات حياتية تقلل من المخاطر المرتبطة بالعوامل البيئية المكتسبة:
أولاً، تجنب التعرض للمواد الكيميائية الصناعية، وتحديداً البنزين ومذيبات الطلاء. إذا كانت طبيعة عملك تتطلب التعامل مع هذه المواد، فإن الالتزام الصارم بارتداء معدات الوقاية الشخصية (PPE) والتهوية الجيدة ليس خياراً، بل ضرورة لحماية نخاعك العظمي.
ثانياً، الإقلاع الفوري عن التدخين. السجائر لا تدمر الرئتين فحسب، بل تحتوي على نسبة من البنزين ومواد مسرطنة تُمتص في مجرى الدم وتزيد من خطر الإصابة بابيضاض الدم النقوي الحاد (AML) كما أشرنا سابقاً.
أخيراً، الحد من التعرض غير الضروري للإشعاع — مثل تجنب طلب صور الأشعة السينية أو المقطعية الطبية إلا عند الضرورة القصوى وبناءً على طلب الطبيب. هذه الخطوات لن تضمن الحماية المطلقة، لكنها تبني درعاً وقائياً يقلل من احتمالات تضرر الحمض النووي (DNA) لخلاياك الجذعية.
كيف يكتشف الطبيب ابيضاض الدم خطوة بخطوة؟
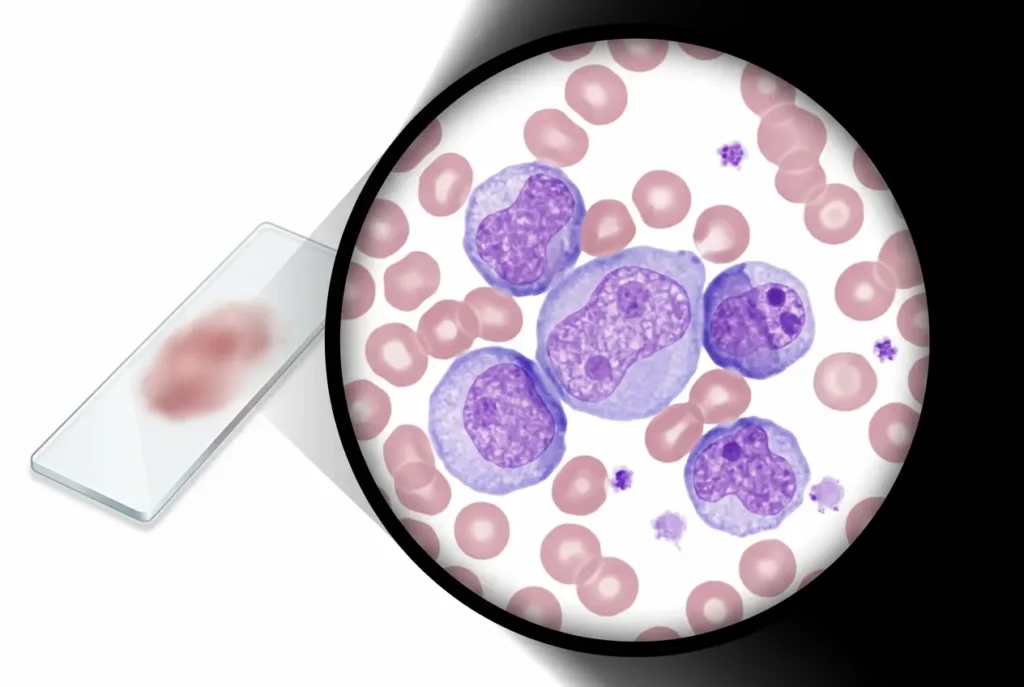
رحلة تشخيص اللوكيميا تبدأ عادةً بتحليل دم بسيط وتنتهي بفحوصات متقدمة ترسم صورة جينية دقيقة للمرض. كل خطوة مبنية على ما قبلها، والطبيب لا يُشخّص بقفزة واحدة بل بسلسلة منطقية من الفحوصات.
الخطوة الأولى: الفحص السريري والتاريخ الطبي. يسأل الطبيب عن الأعراض ومدتها، ويفحص العقد اللمفاوية والطحال والكبد يدوياً. ثم يطلب تعداد الدم الكامل (Complete Blood Count — CBC) مع مسحة دم محيطية (Peripheral Blood Smear). هذا التحليل يكشف ارتفاعاً أو انخفاضاً غير طبيعي في أعداد الخلايا، ويُظهر تحت المجهر وجود خلايا أرومية (Blasts) لا ينبغي لها أن تكون في الدم المحيطي.
الخطوة الحاسمة: خزعة نخاع العظم (Bone Marrow Biopsy). هذا هو الإجراء الذهبي لتشخيص سرطان الدم. يأخذ الطبيب عينة من نخاع العظم — عادةً من عظم الحوض الخلفي — تحت تخدير موضعي. العيّنة تُفحص تحت المجهر لتحديد نسبة الأرومات ونوع الخلايا المصابة. إذا تجاوزت نسبة الأرومات 20% من خلايا النخاع، فهذا يُؤكّد عادةً تشخيص اللوكيميا الحادة.
لكن التشخيص لا يتوقف هنا. تُجرى فحوصات التدفق الخلوي (Flow Cytometry) التي تُحدّد نوع البروتينات على سطح الخلايا السرطانية — وهذا ما يميّز النوع الليمفاوي من النقوي. ثم تأتي الفحوصات الجينية الخلوية (Cytogenetics) وفحوصات FISH (Fluorescence In Situ Hybridization) للبحث عن تغيّرات كروموسومية محددة مثل كروموسوم فيلادلفيا. وأخيراً، فحوصات البيولوجيا الجزيئية (Molecular Studies) بتقنية PCR للبحث عن طفرات جينية بعينها مثل FLT3 وNPM1 وIDH1/2 في AML.
معلومة سريعة: خزعة نخاع العظم قد تبدو مخيفة في الاسم، لكنها إجراء يتم في العيادة ويستغرق عادةً 15 إلى 20 دقيقة فقط. معظم المرضى يصفون الألم بأنه ضغط عميق قصير المدة. التخدير الموضعي يجعل الإجراء محتملاً تماماً.
بعد اكتمال التشخيص، تُجرى فحوصات تصويرية مثل الأشعة المقطعية (CT Scan) أو التصوير بالرنين المغناطيسي (MRI) للبحث عن تضخم في الأعضاء أو ارتشاح سرطاني خارج نخاع العظم. في بعض الحالات يُطلب بزل قطني (Lumbar Puncture) لفحص السائل الشوكي والتأكد من عدم وصول الخلايا السرطانية إلى الجهاز العصبي.
ما الخيارات العلاجية المتاحة وكيف أحدث الطب الحديث ثورة في مواجهة اللوكيميا؟
⚠️ تحذير مهم: جميع الأدوية والجرعات المذكورة في هذا القسم لأغراض تثقيفية فقط. لا تبدأ أو تُوقف أو تُعدّل أي دواء بنفسك. الطبيب المعالج هو الوحيد المخوّل بوصف العلاج وتحديد الجرعة المناسبة لحالتك.
العلاج الكيميائي (Chemotherapy)
يبقى العلاج الكيميائي حجر الأساس في علاج معظم أنواع اللوكيميا الحادة. يعمل عن طريق استهداف الخلايا سريعة الانقسام — سواء كانت سرطانية أم طبيعية — ولهذا تأتي آثاره الجانبية من إصابة الخلايا الطبيعية سريعة الانقسام كخلايا الشعر وبطانة الجهاز الهضمي.
بروتوكول علاج ابيضاض الدم الليمفاوي الحاد (ALL) عند الأطفال يتضمن عادةً ثلاث مراحل: مرحلة الحث (Induction) تهدف لتحقيق الهدأة الكاملة خلال 4 أسابيع باستخدام مزيج من فينكريستين (Vincristine) ودواء كورتيكوستيرويدي مثل ديكساميثازون (Dexamethasone) وأسباراجيناز (Asparaginase) مع داونوروبيسين (Daunorubicin). ثم مرحلة التكثيف (Consolidation) التي تستخدم أدوية مختلفة لقتل أي خلايا متبقية. وأخيراً مرحلة الصيانة (Maintenance) التي قد تمتد لسنتين أو ثلاث باستخدام ميثوتركسات (Methotrexate) و6-ميركابتوبيورين (6-Mercaptopurine) بجرعات يومية أو أسبوعية.
أما في ابيضاض الدم النقوي الحاد (AML) عند البالغين، فالبروتوكول التقليدي يُعرف بـ “7+3” — سبعة أيام من سيتارابين (Cytarabine) المتواصل عبر الوريد مع ثلاثة أيام من داونوروبيسين أو إيداروبيسين (Idarubicin).
يُشير المستشار الدوائي جاسم محمد مراد — خبير الصحة والإمداد الطبي في موقع وصفة طبية — إلى أن “المريض يجب أن يخبر فريقه الطبي بكل دواء أو مكمّل يتناوله، بما في ذلك المكملات العشبية والفيتامينات، لأن بعضها قد يتعارض مع العلاج الكيميائي ويُقلّل فعاليته أو يزيد سُمّيته. مثلاً، مكملات فيتامين C بجرعات عالية قد تتداخل مع بعض أدوية العلاج الكيميائي.”
الآثار الجانبية الشائعة للعلاج الكيميائي:
تشمل الغثيان والقيء، وتساقط الشعر، وتقرحات الفم، وانخفاض شديد في تعداد خلايا الدم (Pancytopenia) — وهو أخطر أثر جانبي لأنه يُعرّض المريض لعدوى قد تكون مهدّدة للحياة. يُعطى المريض عادةً أدوية مضادة للغثيان مثل أوندانسيترون (Ondansetron) وعوامل محفّزة لنمو خلايا الدم مثل فيلغراستيم (Filgrastim — G-CSF) لتقصير فترة نقص المناعة.
فرط الجرعة: تُحسب جرعات العلاج الكيميائي بدقة شديدة بناءً على مساحة سطح الجسم (BSA) أو الوزن، ويتم إعطاؤها في المستشفى تحت إشراف مباشر. أي خطأ في الجرعة يمكن أن يكون قاتلاً، ولهذا يُراجع الصيدلي السريري كل وصفة قبل تحضيرها.
| الدواء | النوع العلاجي | نوع اللوكيميا | الهدف الجزيئي | طريقة الإعطاء |
|---|---|---|---|---|
| إيماتينيب (Imatinib) | مثبط TKI — الجيل الأول | CML / ALL (Ph+) | BCR-ABL1 | فموي — 400 ملغ / يومياً |
| نيلوتينيب (Nilotinib) | مثبط TKI — الجيل الثاني | CML | BCR-ABL1 | فموي — 300 ملغ / مرتين يومياً |
| فينيتوكلاكس (Venetoclax) | مثبط BCL-2 | AML / CLL | BCL-2 (موت خلوي مبرمج) | فموي — جرعة تدريجية |
| بليناتوموماب (Blinatumomab) | جسم مضاد ثنائي الخصوصية | ALL (B-cell) | CD3 / CD19 | وريدي مستمر |
| تيساجينليكلوسيل (Kymriah) | خلايا CAR-T | ALL (الأطفال والشباب) | CD19 | جرعة وريدية واحدة |
| ميدوستورين (Midostaurin) | مثبط FLT3 | AML (FLT3+) | FLT3 | فموي — مع العلاج الكيميائي |
| إبروتينيب (Ibrutinib) | مثبط BTK | CLL | BTK (Bruton’s Kinase) | فموي — 420 ملغ / يومياً |
العلاج الموجّه (Targeted Therapy)
إذا كان العلاج الكيميائي مثل قصف عشوائي يُصيب كل ما يتحرك، فالعلاج الموجّه مثل صاروخ ذكي يُصيب هدفاً واحداً بعينه. هذه الأدوية تستهدف بروتيناً أو مساراً جزيئياً محدّداً موجوداً في الخلايا السرطانية ولا يوجد (أو يوجد بنسبة أقل) في الخلايا الطبيعية.
أمثلة رئيسة:
- مثبطات التيروزين كيناز (TKIs) لعلاج CML: إيماتينيب (Imatinib) 400 ملغ يومياً عن طريق الفم هو الخط الأول. إذا لم يستجب المريض أو ظهرت مقاومة، يُنتقل إلى الجيل الثاني: نيلوتينيب (Nilotinib) 300 ملغ مرتين يومياً أو داساتينيب (Dasatinib) 100 ملغ مرة يومياً. الجيل الثالث بوناتينيب (Ponatinib) يُستخدم للحالات المقاومة بما فيها طفرة T315I.
- مثبطات FLT3 لعلاج AML: ميدوستورين (Midostaurin) يُضاف للعلاج الكيميائي في حالات AML الحاملة لطفرة FLT3. وغيلتيرتينيب (Gilteritinib) يُستخدم كخط ثانٍ.
- مثبطات IDH لعلاج AML: إيناسيدينيب (Enasidenib) لطفرة IDH2 وإيفوسيدينيب (Ivosidenib) لطفرة IDH1.
- فينيتوكلاكس (Venetoclax): مثبط BCL-2 الذي يُعيد تفعيل الموت الخلوي المبرمج. أُضيف إلى علاج CLL وأيضاً إلى بروتوكولات AML لكبار السن غير المؤهلين للعلاج الكيميائي المكثف.
صندوق الاقتباس الطبي (Medical Call-out Box):
وفقاً لـ إدارة الغذاء والدواء الأميركية (FDA), وافقت الإدارة بين عامي 2017 و2024 على أكثر من 15 دواءً جديداً لعلاج أنواع مختلفة من اللوكيميا، مما يعكس التسارع غير المسبوق في البحث والتطوير الدوائي لسرطانات الدم.
العلاج المناعي (Immunotherapy)
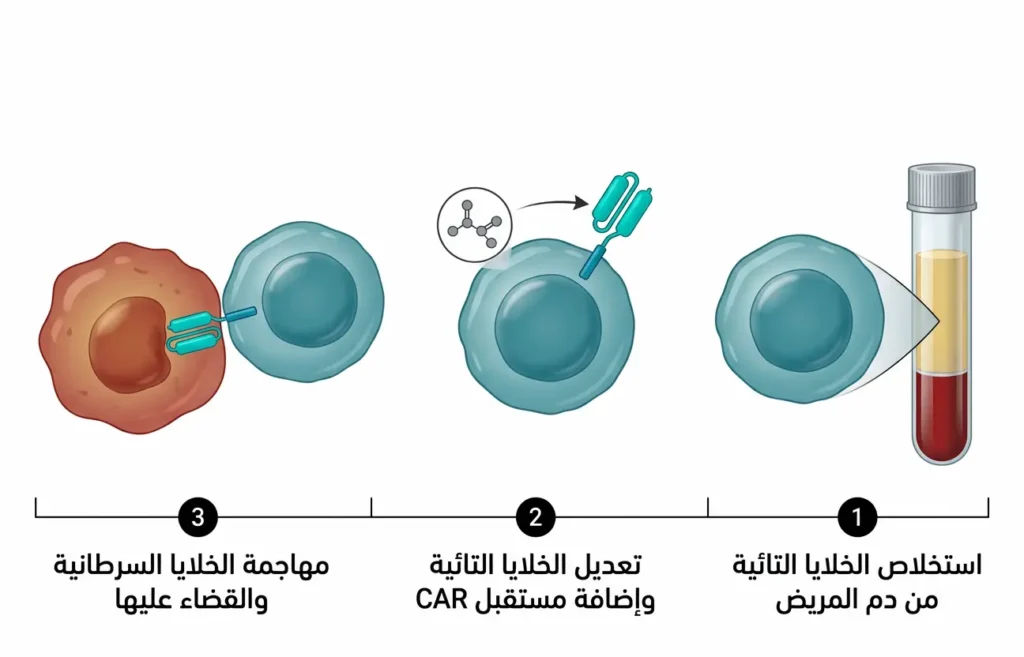
العلاج المناعي يُسخّر جهاز المناعة نفسه — جيش الدفاع الطبيعي في جسمك — ليتعرّف على الخلايا السرطانية ويُهاجمها. فبدلاً من إعطاء الجسم سلاحاً خارجياً، تُدرّبه على استخدام أسلحته الخاصة.
أبرز أنواع العلاج المناعي للوكيميا:
- الأجسام المضادة وحيدة النسيلة (Monoclonal Antibodies): ريتوكسيماب (Rituximab) يستهدف بروتين CD20 على سطح الخلايا الليمفاوية البائية ويُستخدم في بعض حالات CLL وALL. بليناتوموماب (Blinatumomab) — وهو جسم مضاد ثنائي الخصوصية (Bispecific Antibody) — يربط بين الخلية التائية والخلية السرطانية البائية (عبر CD3 وCD19) فيُوجّه الخلية المناعية لقتل السرطانية مباشرة.
- العلاج بخلايا CAR-T (Chimeric Antigen Receptor T-cell Therapy): هذا هو أحد أكثر الابتكارات إثارة في تاريخ الطب الحديث. تُسحب الخلايا التائية من دم المريض وتُعدَّل جينياً في المختبر لتحمل مستقبلاً اصطناعياً يتعرّف على بروتين CD19 الموجود على الخلايا السرطانية، ثم تُعاد إلى جسم المريض لتُباشر مهاجمة السرطان. وافقت FDA على عدة منتجات CAR-T لعلاج ALL المنتكس عند الأطفال والشباب، منها تيساجينليكلوسيل (Tisagenlecleucel) المعروف تجارياً بـ كيمريا (Kymriah).
من المثير أن تعرف: في التجارب السريرية الأولى لعلاج CAR-T عام 2012 في مستشفى الأطفال بفيلادلفيا، كانت إميلي وايتهيد — أول طفلة تتلقى هذا العلاج — قد فقدت كل أمل بعد انتكاسات متعددة من ALL. بعد CAR-T، دخلت في هدأة كاملة ولا تزال خالية من المرض حتى اليوم بعد أكثر من 13 عاماً.
الآثار الجانبية للعلاج المناعي:
أبرزها متلازمة إطلاق السيتوكينات (Cytokine Release Syndrome — CRS) التي تظهر بعد علاج CAR-T وتشمل حمّى شديدة وانخفاض ضغط الدم وصعوبة التنفس. تُعالج عادةً بعقار توسيليزوماب (Tocilizumab). كذلك قد تحدث سُمّية عصبية (Neurotoxicity) تتضمن ارتباكاً وصعوبة في الكلام وتشنجات. كلا الأثرين قابلان للعلاج في الغالب إذا رُصدا مبكراً.
زراعة الخلايا الجذعية (نخاع العظم)
زراعة نخاع العظم (Bone Marrow Transplant) — أو بالأدق زراعة الخلايا الجذعية المكوّنة للدم (Hematopoietic Stem Cell Transplantation — HSCT) — تُعَدُّ الخيار العلاجي الأكثر كثافة، وتُستخدم عندما يكون المرض عالي الخطورة أو منتكساً أو لم يستجب للعلاجات الأولى.
الفكرة ببساطة: يُعطى المريض علاجاً كيميائياً أو إشعاعياً مكثفاً لتدمير نخاع العظم المريض بالكامل، ثم تُزرع فيه خلايا جذعية سليمة من متبرع مطابق (Allogeneic Transplant) أو من المريض نفسه (Autologous Transplant) لإعادة بناء نخاع عظم جديد وصحي.
التحدي الأكبر في الزراعة من متبرع هو مرض الطعم ضد المضيف (Graft-versus-Host Disease — GvHD) الذي يحدث عندما تُهاجم الخلايا المناعية المزروعة أنسجة المريض. لكن هذا التأثير — بشكل معتدل — قد يكون مفيداً، لأنه يعني أن الخلايا المناعية الجديدة تُهاجم أيضاً أي خلايا سرطانية متبقية — وهذا ما يُسمّى تأثير الطعم ضد اللوكيميا (Graft-versus-Leukemia — GvL).
تُشير الدكتورة سوزان عبد الحميد السعدي — استشارية أمراض الدم وزرع الخلايا الجذعية في موقع وصفة طبية — إلى أن “العثور على متبرع مطابق كان يُمثّل عقبة كبيرة في الماضي، لكن تقنيات الزراعة نصف المتطابقة (Haploidentical Transplant) من أحد الوالدين أو الأبناء قد وسّعت بشكل كبير خيارات المرضى الذين لا يملكون شقيقاً مطابقاً. كما أن استخدام سيكلوفوسفاميد بعد الزرع (Post-Transplant Cyclophosphamide) قلّل نسب GvHD الشديد بشكل ملحوظ.”
في السعودية، تتوفر مراكز متقدمة لزراعة الخلايا الجذعية مثل مستشفى الملك فيصل التخصصي ومركز الأبحاث في الرياض وجدة، وهو من المراكز المصنّفة عالمياً في هذا المجال. برنامج زراعة نخاع العظم السعودي أجرى آلاف الزراعات بنسب نجاح تُنافس المراكز الأوروبية والأميركية.
خرافات شائعة وحقائق علمية عن اللوكيميا
❌ الخرافة: اللوكيميا مرض قاتل لا شفاء منه.
✅ الحقيقة: نسبة الشفاء التام من ابيضاض الدم الليمفاوي الحاد عند الأطفال تتجاوز 90%، ونسبة البقاء طويل الأمد في CML مع العلاج الموجّه تتجاوز 85%. لقد تغيّر واقع المرض جذرياً. (المصدر: الجمعية الأميركية للسرطان)
❌ الخرافة: سرطان الدم ينتقل بالعدوى من شخص لآخر.
✅ الحقيقة: اللوكيميا ليست مرضاً معدياً على الإطلاق. لا ينتقل بالمخالطة أو الملامسة أو مشاركة الطعام. هو خلل في الخلايا الجذعية داخل نخاع عظم الشخص نفسه.
❌ الخرافة: إذا كان أحد أفراد عائلتي مصاباً فسأُصاب حتماً.
✅ الحقيقة: الغالبية العظمى من حالات اللوكيميا ليست وراثية. وجود تاريخ عائلي قد يرفع الاستعداد قليلاً في بعض الأنواع النادرة، لكنه لا يعني حتمية الإصابة. (المصدر: المعهد الوطني للسرطان — NCI)
❌ الخرافة: العلاج الكيميائي أسوأ من المرض نفسه.
✅ الحقيقة: رغم صعوبة الآثار الجانبية، فإن العلاج الكيميائي يُنقذ حياة الملايين. الأدوية المساندة الحديثة المضادة للغثيان والمحفّزة لنمو خلايا الدم جعلت التحمّل أفضل بكثير مما كان عليه قبل عقدين.
❌ الخرافة: الأعشاب والطب البديل يمكن أن تشفي من سرطان الدم دون علاج طبي.
✅ الحقيقة: لا يوجد أي دليل علمي موثوق يُثبت أن أي عشبة أو مكمّل طبيعي يمكنه شفاء اللوكيميا. التأخر عن العلاج الطبي بسبب الاعتماد على العلاجات البديلة وحدها قد يكون قراراً قاتلاً.
كيف يتعايش مريض اللوكيميا مع العلاج ويحمي نفسه خلاله؟
التعايش مع تشخيص سرطان الدم ليس مجرد تحدٍّ جسدي؛ إنه رحلة نفسية واجتماعية تحتاج إلى دعم منظّم. دعني أتحدث معك عن الجوانب العملية التي تصنع فارقاً حقيقياً في جودة حياة المريض.
الدعم النفسي ليس ترفاً. دراسة نُشرت في مجلة Journal of Clinical Oncology عام 2021 أظهرت أن المرضى الذين تلقّوا دعماً نفسياً منظّماً إلى جانب العلاج الطبي أظهروا التزاماً أعلى بالبروتوكول العلاجي ونسب استجابة أفضل مقارنة بمن لم يتلقّوا هذا الدعم. الخوف والقلق والاكتئاب ليست “ضعفاً”؛ بل هي استجابة طبيعية لخبر مروّع، والاعتراف بها أول خطوات التعامل معها.
في أثناء فترات العلاج الكيميائي، ينخفض عدد خلايا الدم البيضاء (Neutropenia) وتضعف المناعة بشكل حاد. هذه الفترة — التي تُسمّى فترة النقص — هي الأكثر حساسية ويحتاج فيها المريض إلى اتخاذ احتياطات صارمة لتجنب العدوى.
نقطة تستحق الانتباه: في المملكة العربية السعودية، توفّر العديد من المستشفيات الحكومية والخاصة فرق دعم نفسي متكاملة لمرضى السرطان، بما في ذلك جلسات إرشاد فردية وجماعية. لا تتردد في السؤال عن هذه الخدمات عند بدء العلاج.
اقرأ أيضاً:
إلى مقدمي الرعاية (الأهل والأصدقاء): كيف تدعمون المريض دون أن تحترقوا نفسياً؟
غالباً ما يكون تشخيص اللوكيميا زلزالاً يضرب الأسرة بأكملها، وليس المريض وحده. إذا كنت تقرأ هذا المقال لأن ابناً أو زوجاً أو أباً لك قد شُخّص بالمرض، فهذه الفقرة مخصصة لك. أنت الجندي المجهول في هذه المعركة، ودورك لا يقل أهمية عن دور الفريق الطبي.
أولاً، اسمح لنفسك بالشعور بالضعف. الإرهاق النفسي أو ما يُعرف بـ “إرهاق مقدم الرعاية” (Caregiver Burnout) حالة طبية معترف بها. لا تكبت حزنك أو خوفك لتظهر “قوياً” طوال الوقت، فجسمك سيترجم هذا الكبت إلى أمراض جسدية.
ثانياً، قسّم المهام ولا تكن البطل الأوحد. اطلب من الأقارب أو الأصدقاء تولي مهام محددة: توصيل الأطفال للمدرسة، تحضير وجبات آمنة ومناسبة، أو حتى البقاء مع المريض لبضع ساعات لتتمكن من أخذ قيلولة أو الخروج لاستنشاق هواء نقي. المريض يحتاجك بصحة جيدة وذهن صافٍ، فإذا انهرت أنت، من سيسنده؟
وأخيراً، عندما تتحدث مع المريض، لا تضغط عليه بعبارات الإيجابية المفرطة مثل “يجب أن تكون سعيداً وتضحك لتهزم المرض”. من حقه أن يغضب ويبكي. أفضل ما يمكنك فعله هو أن تكون مستمعاً متعاطفاً، وأن تقول له ببساطة: “أنا هنا، وسنعبر هذا النفق معاً خطوة بخطوة”.
ماذا يأكل مريض اللوكيميا لحماية مناعته في أثناء العلاج؟

⚠️ تحذير: هذه الفقرة لأغراض تثقيفية ولا تُغني عن استشارة اختصاصي تغذية يُراعي الحالة الفردية للمريض ونوع العلاج الذي يتلقاه.
التغذية لمريض ابيضاض الدم ليست مجرد “أكل صحي” عام؛ بل هي جزء من بروتوكول حماية المناعة في أثناء فترات العلاج الكيميائي. الهدف الأول هو تجنّب العدوى المنقولة بالطعام (Foodborne Infections) لأن الجهاز المناعي يكون في أضعف حالاته.
النظام الغذائي الآمن (Neutropenic Diet) يعتمد على طهي جميع الأطعمة جيداً وتجنب الأطعمة النيئة مثل السوشي والسلطات غير المغسولة والبيض النيئ والحليب غير المبستر. يُركّز على البروتينات عالية الجودة كالدجاج واللحم المطهو جيداً والأسماك المطبوخة والبيض المطهو بالكامل. الفواكه تؤكل بعد غسلها جيداً وتقشيرها. الخضروات تُطهى ولا تُؤكل نيئة في أثناء فترات النقص المناعي.
يحتاج مريض اللوكيميا أيضاً إلى سعرات حرارية كافية — قد تصل إلى 25-30 سعرة حرارية لكل كيلوغرام من الوزن يومياً — لتعويض ما يستنزفه المرض والعلاج. البروتين ضروري لإعادة بناء الأنسجة والخلايا المناعية: يُنصح بـ 1.2 إلى 1.5 غرام من البروتين لكل كيلوغرام يومياً.
تنصح الدكتورة علا الأحمد — اختصاصية التغذية العلاجية في موقع وصفة طبية — بأن “مريض اللوكيميا يجب أن يتناول وجبات صغيرة ومتعددة (5-6 وجبات يومياً) بدلاً من ثلاث وجبات كبيرة، خاصة إذا كان يعاني من الغثيان. الأطعمة الغنية بالزنك مثل اللحوم الحمراء والحمّص وبذور اليقطين تدعم المناعة بشكل مباشر. والحفاظ على ترطيب الجسم بشرب 2 إلى 2.5 لتر من الماء يومياً — ما لم يمنع الطبيب ذلك — يُساعد الكلى على التخلص من نواتج العلاج الكيميائي.”
للأطفال المصابين: قد يرفض الطفل الطعام بسبب تقرحات الفم أو الغثيان. يُفضّل تقديم أطعمة باردة أو بدرجة حرارة الغرفة (الأيسكريم المبستر، الزبادي، العصائر المطبوخة) لأنها ألطف على الفم. يمكن إضافة بودرة بروتين مخصّصة للأطفال بتوجيه من اختصاصي التغذية.
لكبار السن: قد يعانون من فقدان شهية أشد ومن صعوبات في البلع. يُنصح بزيادة كثافة السعرات في كميات صغيرة — مثل إضافة زيت الزيتون إلى الأطباق أو استخدام مكمّلات غذائية سائلة عالية السعرات تحت إشراف طبي.
اقرأ أيضاً:
- حاسبة السعرات الحرارية اليومية حسب العمر والوزن والطول والنشاط
- حاسبة البروتين اليومي: احسب احتياجك اليومي من البروتين
ما دور المكملات الغذائية والأعشاب — وأين يكمن الخطر؟
⚠️ تحذير مهم: لا تتناول أي مكمّل غذائي أو عشبي في أثناء علاج اللوكيميا دون مراجعة الطبيب المعالج أو الصيدلي السريري. بعض المكملات قد تتعارض تعارضاً خطيراً مع أدوية العلاج الكيميائي أو الموجّه.
كثير من المرضى والأهالي — خاصة في مجتمعاتنا العربية — يبحثون عن “شيء إضافي” يمكنهم فعله إلى جانب العلاج الطبي. هذا الشعور طبيعي ومفهوم، لكنه يحتاج إلى توجيه دقيق. دعني أراجع معك أبرز المكملات التي يسأل عنها المرضى.
الكركم (Curcumin): يُشاع أن الكركمين يملك خصائص مضادة للسرطان. في المختبر نعم، أظهرت بعض الدراسات تأثيراً مُثبّطاً على بعض خطوط الخلايا السرطانية. لكن هناك مشكلة حقيقية: الكركمين قد يُثبّط إنزيمات السيتوكروم P450 (CYP450) في الكبد — وهي نفس الإنزيمات التي تُستقلب (تُكسّر) كثيراً من أدوية العلاج الكيميائي والموجّه مثل إيماتينيب ونيلوتينيب. وعليه فإن تناول مكملات الكركم المركّزة قد يُغيّر تركيز الدواء في الدم ويجعله إما سامّاً أو غير فعّال. ماذا تفعل؟ استخدام الكركم كتوابل في الطعام بكميات عادية لا يُشكّل خطراً. المشكلة في المكملات عالية الجرعة (500 ملغ فأكثر). إذا كنت تتناولها، أخبر طبيبك فوراً.
الزنجبيل (Ginger): يُستخدم تقليدياً لتخفيف الغثيان. دراسة في مجلة Supportive Care in Cancer عام 2019 أشارت إلى أن الزنجبيل بجرعات صغيرة (250-500 ملغ قبل الوجبات) قد يُساعد في تخفيف الغثيان المرتبط بالعلاج الكيميائي. لكن الزنجبيل يملك خاصية مضادة لتجمّع الصفائح الدموية (Antiplatelet Effect)، وهذا خطر حقيقي لمريض اللوكيميا الذي يعاني أصلاً من نقص الصفائح. ماذا تفعل؟ لا تتناوله كمكمّل إذا كان عدد صفائحك أقل من 50,000/ميكرولتر. استشر طبيبك أولاً.
الثوم (Garlic): يُشاع أنه “مضاد حيوي طبيعي”. لكنه يُثبّط تجمّع الصفائح الدموية أيضاً ويتداخل مع أدوية السيولة إن وُصفت. كما يُثبّط CYP3A4 مما يؤثر على استقلاب بعض أدوية العلاج الموجّه. ماذا تفعل؟ الثوم في الطبخ بكميات طبيعية آمن. مكملات الثوم المركّزة ممنوعة في أثناء العلاج.
فيتامين D: نقص فيتامين D شائع جداً عند مرضى سرطان الدم. مستوياته المنخفضة ارتبطت بسوء المآل في بعض الدراسات. تعويضه بجرعة 1000-2000 وحدة دولية يومياً آمن في الغالب، لكن يجب فحص مستواه أولاً وضبط الجرعة بناءً على النتيجة. لا تتجاوز 4000 وحدة دولية يومياً دون إشراف طبي.
الجنسنج (Ginseng): بعض أنواعه تمتلك خصائص مُعزّزة للمناعة. لكنها قد تتداخل مع أدوية العلاج المناعي عبر تعديل نشاط الخلايا القاتلة الطبيعية (NK Cells) والسيتوكينات بطريقة غير متوقعة. ماذا تفعل؟ تجنّبه تماماً في أثناء العلاج المناعي أو CAR-T.
يُؤكّد المستشار الدوائي جاسم محمد مراد أن “القاعدة الذهبية لأي مريض سرطان دم هي: لا تُضف أي شيء إلى فمك — سواء كان مكملاً أو عشبة أو فيتاميناً — دون أن يعرف فريقك الطبي. احمل قائمة مكتوبة بكل ما تتناوله وأرِها لطبيبك والصيدلي في كل زيارة.”
هل يمكن أن تكون أعراض اللوكيميا مؤشراً لأمراض أخرى في الجسم؟
الأعراض التي تُرافق سرطان الدم — كالتعب المزمن والكدمات والعدوى المتكررة — ليست حكراً عليه. فهم هذا التداخل مهم لأنه يمنع التشخيص الخاطئ ويدفعك إلى الفحص الشامل. فما هي الأمراض الأخرى التي قد تختبئ خلف هذه الأعراض؟
فقر الدم اللاتنسجي (Aplastic Anemia): مرض يُصيب نخاع العظم ويُقلّل إنتاج جميع أنواع خلايا الدم — تماماً كاللوكيميا — لكنه ليس سرطاناً. السبب غالباً مناعي ذاتي (Autoimmune) أو سُمّي. التمييز يتم عبر خزعة نخاع العظم التي تكشف نقص الخلوية (Hypocellularity) بدلاً من تكاثر الأرومات.
متلازمات خلل التنسج النقوي (Myelodysplastic Syndromes — MDS): مجموعة اضطرابات في نخاع العظم تُنتج خلايا دم غير طبيعية. تُعَدُّ حالة سابقة للسرطان وقد تتحوّل إلى AML في 30% من الحالات تقريباً. التشخيص يعتمد على نسبة الأرومات ونوع خلل التنسج.
أمراض المناعة الذاتية (Autoimmune Diseases): الذئبة الحمامية الجهازية (Systemic Lupus Erythematosus — SLE) والتهاب المفاصل الروماتويدي (Rheumatoid Arthritis) يمكن أن يُسببا نقصاً في خلايا الدم وتضخماً في العقد اللمفاوية وأعراضاً جهازية تُشبه اللوكيميا. الفحوصات المناعية (ANA, Anti-dsDNA) تُساعد في التفريق.
عدوى فيروسية شديدة: بعض الفيروسات مثل فيروس إبشتاين-بار (Epstein-Barr Virus — EBV) والفيروس المضخّم للخلايا (Cytomegalovirus — CMV) يمكن أن تُحدث ارتفاعاً في الخلايا الليمفاوية الشاذة الشكل (Atypical Lymphocytes) قد يُشبه اللوكيميا تحت المجهر. الفحوصات الفيروسية والتدفق الخلوي يكشفان الفرق.
اقرأ أيضاً:
علاج اللوكيميا عند الأطفال: ما الذي يجب أن يعرفه كل أب وأم؟
⚠️ تحذير: هذه المعلومات تثقيفية ولا تُغني عن متابعة طبيب أمراض دم وأورام أطفال مختص.
سرطان الدم عند الأطفال — وتحديداً ابيضاض الدم الليمفاوي الحاد (ALL) — هو أكثر أنواع السرطان شيوعاً في مرحلة الطفولة. لكنه أيضاً أحد أكثر الأنواع قابلية للشفاء. هذه مفارقة مُطمئنة يجب أن يعرفها كل أب وأم.
بروتوكولات العلاج المعتمدة دولياً — مثل بروتوكول COG (Children’s Oncology Group) — تستمر عادةً من سنتين إلى ثلاث سنوات. المرحلة الأولى (الحث) هي الأكثر كثافة وتتطلب عادةً دخولاً متكرراً إلى المستشفى. بعدها يبدأ الطفل مرحلة الصيانة التي تعتمد على أدوية فموية ومتابعة في العيادة.
الأطفال يتحمّلون العلاج الكيميائي بشكل عام أفضل من البالغين. لكن هذا لا يعني أن الطريق سهل. تساقط الشعر والغثيان والعزلة عن المدرسة والأصدقاء تُشكّل تحديات نفسية حقيقية. في السعودية، تُوفّر عدة مستشفيات — مثل مستشفى الملك فيصل التخصصي ومدينة الملك فهد الطبية — برامج تعليمية داخل المستشفى تُمكّن الطفل من مواصلة دراسته في أثناء العلاج. كذلك تُقدّم جمعيات مثل جمعية أصدقاء مرضى السرطان دعماً مادياً ونفسياً للأسرة.
هل تعلم؟ في خمسينيات القرن الماضي كانت نسبة الشفاء من ALL عند الأطفال أقل من 10%. اليوم تتجاوز 90% في المراكز المتقدمة. هذا التحوّل الهائل جاء نتيجة عقود من الأبحاث السريرية وتطوير البروتوكولات العلاجية المتعددة الأدوية.
نقطة مهمة للأهل: بعد انتهاء العلاج، يحتاج الطفل إلى متابعة طويلة الأمد (Long-Term Follow-Up) لرصد أي آثار متأخرة للعلاج الكيميائي أو الإشعاعي، مثل مشكلات القلب أو الغدد الصمّاء أو صعوبات التعلم. لا تتوقف عن المتابعة بعد إعلان الشفاء.
اقرأ أيضاً:
كيف يتعامل كبار السن وأصحاب الأمراض المزمنة مع تشخيص اللوكيميا؟
كبار السن (فوق 65 عاماً) يُشكّلون الشريحة الأكبر من مرضى ابيضاض الدم النقوي الحاد (AML) وابيضاض الدم الليمفاوي المزمن (CLL). لكن علاجهم يختلف عن الشباب لأن أجسامهم أقل تحمّلاً للعلاج الكيميائي المكثف، وكثير منهم يعانون من أمراض مزمنة مصاحبة مثل السكري وأمراض القلب والكلى.
لهذا السبب، طُوّرت بروتوكولات أقل كثافة ولكن فعّالة. فينيتوكلاكس (Venetoclax) مع أزاسيتيدين (Azacitidine) أصبح الخط الأول لعلاج AML عند كبار السن غير المؤهلين للعلاج المكثف، وقد أظهر نتائج واعدة في دراسة VIALE-A المنشورة في New England Journal of Medicine عام 2020 — نسبة الهدأة الكاملة بلغت 66% مقارنة بـ 28% مع أزاسيتيدين وحده.
أما في CLL، فمعظم المرضى كبار السن لا يحتاجون إلى علاج فوري؛ بل يُتابَعون بالمراقبة. وعندما يحتاجون إلى علاج، يُستخدم إبروتينيب (Ibrutinib) أو أكالابروتينيب (Acalabrutinib) — وهي مثبطات BTK (Bruton’s Tyrosine Kinase) — بجرعة فموية يومية دون حاجة إلى دخول المستشفى. لكن يجب الانتباه إلى أن إبروتينيب قد يُسبّب رجفاناً أذينياً (Atrial Fibrillation) وارتفاع ضغط الدم ونزيفاً، مما يستدعي متابعة قلبية دقيقة عند المرضى المصابين بأمراض القلب.
لأصحاب الأمراض المزمنة: إذا كنت مصاباً بالسكري وتتلقى علاجاً كيميائياً يتضمن ديكساميثازون أو بريدنيزولون (وهي كورتيكوستيرويدات ترفع السكر بشدة)، فستحتاج إلى ضبط جرعات الأنسولين أو أدوية السكري الفموية بدقة في أثناء فترات العلاج. أخبر طبيب السكري قبل بدء العلاج الكيميائي واطلب خطة مشتركة.
اقرأ أيضاً:
علاج اللوكيميا في الحوامل والمرضعات: بين المسموح والممنوع
⚠️ تحذير طبي ضروري: تشخيص اللوكيميا في أثناء الحمل يتطلب فريقاً طبياً متعدد التخصصات يضم طبيب أورام وطبيب توليد عالي الخطورة واختصاصي أمراض دم. لا يُتّخذ أي قرار علاجي دون تقييم دقيق للمخاطر على الأم والجنين.
اللوكيميا في أثناء الحمل نادرة — تُقدَّر بحالة واحدة من كل 75,000 إلى 100,000 حالة حمل. لكنها تضع الأطباء أمام معادلة صعبة: إنقاذ حياة الأم مع حماية الجنين.
المسموح (نسبياً):
في الثلث الثاني والثالث من الحمل، يمكن إعطاء بعض أدوية العلاج الكيميائي مثل داونوروبيسين وسيتارابين بأمان نسبي، إذ تُظهر البيانات أن الخطر على الجنين يكون أقل بكثير بعد تجاوز مرحلة تكوّن الأعضاء (Organogenesis) التي تكتمل بنهاية الأسبوع الثاني عشر.
الممنوع:
في الثلث الأول (أول 12 أسبوعاً)، معظم أدوية العلاج الكيميائي ممنوعة بسبب خطر التشوّهات الخلقية (Teratogenicity). الميثوتركسات (Methotrexate) على وجه الخصوص مُحرَّم قطعياً في أثناء الحمل لأنه يُثبّط حمض الفوليك الضروري لتطور الجنين ويُسبّب تشوهات وإجهاضاً. كذلك مثبطات التيروزين كيناز (مثل إيماتينيب) أظهرت تشوهات جنينية في الدراسات الحيوانية ويُنصح بتجنّبها خلال الحمل كلما أمكن.
بالنسبة للرضاعة: معظم أدوية العلاج الكيميائي والموجّه تُفرز في حليب الأم. لذلك يُنصح عادةً بإيقاف الرضاعة الطبيعية في أثناء العلاج وحتى فترة كافية بعد آخر جرعة (تختلف حسب الدواء). هذا القرار يجب أن يُناقش مع الطبيب بالتفصيل.
كم تكلّف علاجات اللوكيميا — ولماذا يتفاوت السعر؟
تكلفة علاج سرطان الدم تتفاوت تفاوتاً كبيراً بناءً على عدة عوامل، والشفافية حول هذا الموضوع تُساعد المرضى والأسر على التخطيط المالي.
العلاج الكيميائي التقليدي: في أميركا، قد تتراوح تكلفة بروتوكول كامل من ALL بين 100,000 و250,000 دولار. في السعودية، يُغطّي التأمين الصحي الحكومي ومستشفيات وزارة الصحة والمستشفيات العسكرية تكاليف العلاج بالكامل للمواطنين السعوديين. أما في المستشفيات الخاصة، فقد تتراوح تكلفة الجلسة الواحدة من العلاج الكيميائي بين 3,000 و15,000 ريال سعودي حسب نوع الأدوية.
العلاج الموجّه: إيماتينيب (الشكل العام / Generic) أصبح أقل تكلفة بكثير بعد انتهاء براءة الاختراع، لكن أدوية الجيل الثاني والثالث مثل بوناتينيب قد تصل تكلفتها إلى 15,000 دولار شهرياً في أميركا.
علاج CAR-T: يُعَدُّ الأغلى؛ إذ تتراوح تكلفته بين 373,000 و475,000 دولار لجرعة واحدة في أميركا. في السعودية، بدأت بعض المراكز المتقدمة تقديم هذا العلاج، والتكلفة عادةً تُغطّى عبر برامج التأمين الحكومي أو الصناديق الخيرية.
زراعة نخاع العظم: تتراوح بين 150,000 و800,000 دولار في أميركا حسب نوع الزراعة والمضاعفات. في السعودية، مستشفى الملك فيصل التخصصي يُجري الزراعة بتغطية حكومية كاملة للمواطنين.
العوامل المؤثرة في تفاوت السعر:
- نوع اللوكيميا ومرحلتها — الحادة تحتاج علاجاً أكثف وأطول.
- الأدوية المستخدمة — الأدوية الحديثة والبيولوجية أغلى بكثير.
- المضاعفات — العدوى والحاجة للعناية المركزة ترفع التكلفة.
- المستشفى والبلد — تفاوت كبير بين الدول والمرافق الصحية.
- التأمين الصحي — يُحدث فارقاً جوهرياً في العبء المالي.
ما نسب الشفاء من اللوكيميا وهل تحسّنت فعلاً؟
هذا هو السؤال الذي يدور في ذهن كل مريض وكل أسرة: ما هي نسبة الشفاء من اللوكيميا؟ الإجابة تعتمد على النوع والعمر ووقت التشخيص والاستجابة الأولى للعلاج. لكن الأرقام الحديثة مُبشّرة بحق.
ابيضاض الدم الليمفاوي الحاد (ALL) عند الأطفال: نسبة البقاء على قيد الحياة لخمس سنوات تتجاوز 90% وفقاً لبيانات المعهد الوطني للسرطان الأميركي (NCI). هذا يعني أن 9 من كل 10 أطفال يُشفون شفاءً تاماً.
ابيضاض الدم الليمفاوي الحاد عند البالغين: النسبة أقل — حوالي 40-50% — لكنها تتحسّن مع إضافة العلاجات المناعية الجديدة مثل بليناتوموماب وCAR-T.
ابيضاض الدم النقوي الحاد (AML): نسبة البقاء لخمس سنوات تتراوح بين 25% و30% عموماً، لكنها ترتفع إلى 50-60% في المرضى الأصغر سناً ذوي الطفرات ذات المآل الجيد (Favorable-Risk).
ابيضاض الدم النقوي المزمن (CML): معدل البقاء لعشر سنوات يتجاوز 85% مع العلاج الموجّه بمثبطات TKI. كثير من المرضى يعيشون عمراً طبيعياً تقريباً.
ابيضاض الدم الليمفاوي المزمن (CLL): متوسط البقاء يتجاوز 10 سنوات في معظم الحالات، وكثير من المرضى لا يحتاجون علاجاً لسنوات.
العوامل التي تؤثر على نجاح العلاج:
- العمر: الأطفال يستجيبون أفضل من البالغين وكبار السن.
- نوع اللوكيميا والتغيرات الجينية: بعض الطفرات مرتبطة بمآل أفضل (مثل طفرة NPM1 بدون FLT3 في AML) وبعضها بمآل أسوأ.
- سرعة الاستجابة الأولى: تحقيق الهدأة الكاملة بعد مرحلة الحث الأولى يُعَدُّ مؤشراً إيجابياً قوياً.
- وقت التشخيص: كلما كان التشخيص مبكراً كانت النتائج أفضل.
حقيقة طبية: لقد تضاعفت نسبة البقاء على قيد الحياة لمرضى اللوكيميا عموماً ثلاث مرات تقريباً خلال العقود الأربعة الأخيرة. ما كان يُعَدُّ حكماً بالموت أصبح اليوم مرضاً قابلاً للشفاء في كثير من الحالات.
الخطة العملية للتعامل مع تشخيص اللوكيميا — ورقة تعليمات من طبيبك
- فور سماع التشخيص: خذ نفساً عميقاً. اطلب من طبيبك أن يشرح لك نوع اللوكيميا بالتحديد ومرحلتها والخطة العلاجية المقترحة. دوّن الأسئلة التي تراودك واكتبها في ورقة لتطرحها في الزيارة التالية.
- اختيار المركز العلاجي: تأكد أن المستشفى لديه فريق متخصص في أمراض الدم والأورام وأن لديه خبرة في النوع المحدد من اللوكيميا. في السعودية، المراكز الكبرى كمستشفى الملك فيصل التخصصي ومدينة الملك فهد الطبية ومستشفى الملك عبدالله الجامعي توفر بروتوكولات عالمية.
- قبل بدء العلاج: أجرِ تحاليل الدم الشاملة وفحوصات وظائف القلب (مخطط صدى القلب — Echocardiogram) والكبد والكلى. إذا كنت في سن الإنجاب، ناقش مع طبيبك خيارات حفظ الخصوبة (Fertility Preservation) قبل بدء العلاج الكيميائي.
- خلال فترات العلاج: اغسل يديك بشكل متكرر. تجنّب الأماكن المزدحمة والأشخاص المصابين بعدوى. ارتدِ كمامة في الأماكن العامة. تناول طعاماً مطهواً جيداً. أبلغ فريقك الطبي فوراً عند ارتفاع الحرارة فوق 38 درجة مئوية.
- المتابعة بعد العلاج: حتى بعد تحقيق الهدأة الكاملة، لا تتوقف عن زيارات المتابعة الدورية. فحص نخاع العظم وتحاليل الدم المنتظمة ضرورية لرصد أي انتكاس مبكر.
- الدعم النفسي والاجتماعي: انضم إلى مجموعة دعم مرضى السرطان في منطقتك أو عبر الإنترنت. تحدّث عن مشاعرك. اطلب مساعدة اختصاصي نفسي إذا شعرت بالحاجة. لا تواجه هذا الطريق وحدك.
اقرأ أيضاً:
الوصفة الطبية من موقعنا
هذه ليست نصائح تقليدية تقرؤها في كل مكان. إنها توصيات مبنية على فهم الآليات الفسيولوجية العميقة ومصمّمة لمساعدة جسمك على التعافي والتكيّف.
- احترم إيقاعك اليوماوي (Circadian Rhythm): النوم بين الساعة 10 مساءً و6 صباحاً ليس مجرد عادة صحية؛ بل يُنظّم إفراز هرمون الميلاتونين (Melatonin) الذي يملك خصائص مضادة للأكسدة ومُنظّمة للجهاز المناعي. دراسات حديثة أشارت إلى أن اضطراب النوم المزمن يُخفّض نشاط الخلايا القاتلة الطبيعية (NK Cells) بنسبة تصل إلى 70%. حاول أن تنام في ظلام تام وتتجنب الشاشات قبل النوم بساعة.
- الحركة المنتظمة — حتى لو كانت بسيطة: المشي لمدة 20 إلى 30 دقيقة يومياً — حتى داخل المنزل — يُحفّز إفراز الميوكينات (Myokines) من العضلات، وهي بروتينات إشارية تُثبّط الالتهاب وتدعم تجدّد الخلايا المناعية. لا تحتاج إلى تمارين عنيفة؛ المشي المعتدل كافٍ خاصة في أثناء العلاج.
- التنفس العميق لتهدئة الجهاز العصبي الذاتي: تقنية التنفس البطيء (4 ثوانٍ شهيق — 7 ثوانٍ حبس — 8 ثوانٍ زفير) تُنشّط العصب المبهم (Vagus Nerve) وتُخفّض إفراز الكورتيزول. الكورتيزول المرتفع باستمرار يُثبّط المناعة ويُبطئ التعافي. مارس هذه التقنية مرتين يومياً لمدة 5 دقائق.
- التآزر الغذائي الجزيئي: فيتامين C يُعزّز امتصاص الحديد النباتي (Non-Heme Iron) بنسبة تصل إلى 6 أضعاف. إذا كنت تعاني من فقر الدم المصاحب للعلاج، فتناول مصادر الحديد النباتية (كالسبانخ المطبوخ والعدس) مع عصير ليمون أو فلفل أخضر في الوجبة نفسها. هذا التآزر البسيط يُحدث فارقاً حقيقياً في مستوى الهيموغلوبين.
- تقليل الحِمل الالتهابي عبر الأمعاء: 70% من الجهاز المناعي يقع في الأمعاء (GALT — Gut-Associated Lymphoid Tissue). الحفاظ على تنوّع ميكروبيوم الأمعاء عبر تناول ألياف متنوعة (شوفان، بقوليات مطبوخة، موز ناضج) ومصادر بروبيوتيك مطبوخة آمنة (مثل الزبادي المبستر) يدعم صحة الأمعاء وبالتالي المناعة. تجنّب المحليات الصناعية التي أظهرت بعض الدراسات أنها تُخلّ بتوازن الميكروبيوم.
- التواصل الاجتماعي كأداة علاجية: ليس كلاماً عاطفياً. دراسة نُشرت في مجلة Psychoneuroendocrinology عام 2023 أظهرت أن العزلة الاجتماعية ترفع مستويات الالتهاب الجهازي (CRP, IL-6) وتُثبّط الاستجابة المناعية. تحدّث مع أحبائك. انضم إلى مجتمع داعم. اضحك. هذه أدوات فسيولوجية حقيقية وليست مجرد شعارات.
تؤكّد الدكتورة مها منصور — اختصاصية الأورام والطب النووي في موقع وصفة طبية — أن “العلاج الشامل لمريض اللوكيميا لا يقتصر على الأدوية؛ بل يشمل الدعم النفسي والتغذية والحركة والنوم. المريض الذي يعتني بهذه الجوانب مجتمعة يُظهر استجابة أفضل للعلاج وجودة حياة أعلى بشكل ملحوظ.”
اقرأ أيضاً:
- العبء الالتهابي الجهازي: القاتل الصامت وكيفية إخماده بخطوات طبية مثبتة
- حاسبة النوم حسب العمر
- حاسبة كمية الماء اليومية
علامات الشفاء من سرطان الدم — كيف تعرف أنك على الطريق الصحيح؟
علامات الشفاء من سرطان الدم ليست لحظة واحدة دراماتيكية كما تُصوّرها الأفلام. هي رحلة تدريجية. أول علامة إيجابية هي تحقيق الهدأة الكاملة (Complete Remission — CR)، ويعني أن نسبة الأرومات في نخاع العظم انخفضت إلى أقل من 5% مع عودة تعداد خلايا الدم إلى الحدود الطبيعية واختفاء الأعراض.
الخطوة الأعمق هي الوصول إلى الهدأة الجزيئية (Molecular Remission / Minimal Residual Disease-Negative — MRD-Negative)، حيث لا يمكن اكتشاف أي خلية سرطانية حتى بأكثر الفحوصات حساسية مثل تقنية PCR. تحقيق MRD السلبية يُعَدُّ أقوى مؤشر على شفاء حقيقي ودائم.
بعد ذلك، يمرّ المريض بفترة متابعة طويلة — عادةً 5 سنوات — قبل أن يُعلن الأطباء أنه “خالٍ من المرض” بشكل نهائي. خلال هذه الفترة، تُجرى تحاليل دم دورية وأحياناً خزعات نخاع عظم للتأكد من عدم عودة المرض.
معلومة سريعة: في CML تحديداً، أظهرت دراسات حديثة أن بعض المرضى الذين حققوا هدأة جزيئية عميقة لسنوات يمكنهم التوقف عن تناول مثبطات TKI تحت إشراف طبي دقيق — وبعضهم بقي في هدأة دون علاج. هذا المفهوم يُسمّى “الهدأة الخالية من العلاج” (Treatment-Free Remission — TFR) وهو من أكثر التطورات إثارة.
هاجس الانتكاس: متى يجب أن تقلق بعد إعلان الشفاء؟
حتى بعد الوصول إلى الهدأة الكاملة (Complete Remission) والعودة إلى الحياة الطبيعية، يبقى ظل خفي يطارد معظم المتعافين: الخوف من الانتكاس (Relapse). الانتكاس يعني عودة الخلايا السرطانية للظهور في نخاع العظم أو الدم بعد فترة من اختفائها.
لا نريدك أن تعيش في رعب دائم، لكن الوعي بالجسد أمر بالغ الأهمية. يجب التواصل مع طبيبك المعالج — حتى بين مواعيد المتابعة المجدولة — إذا لاحظت عودة نفس الأعراض التي ظهرت قبل التشخيص الأول، وتحديداً:
- تعب شديد ومفاجئ لا يتحسن بالراحة.
- عودة الكدمات أو النزيف غير المبرر.
- حمى متكررة دون وجود التهاب واضح.
- ألم متجدد في العظام والمفاصل.
إذا حدث الانتكاس — لا سمح الله — تذكر أن الخيارات العلاجية اليوم لا تقف عاجزة. الكثير من العلاجات الحديثة كالعلاج المناعي (CAR-T) وزراعة الخلايا الجذعية، أُقرت خصيصاً كخطوط دفاعية قوية لحالات اللوكيميا المنتكسة، وتستطيع إعادة المريض إلى حالة الهدأة التامة مرة أخرى.
صندوق الاقتباس الطبي:
وفقاً لـ منظمة الصحة العالمية (WHO), فإن سرطانات الدم (بما فيها اللوكيميا واللمفوما والورم النقوي المتعدد) تُشكّل نحو 6% من إجمالي حالات السرطان الجديدة عالمياً، وتُعَدُّ اللوكيميا الأكثر شيوعاً بين سرطانات الأطفال. لكن التحسّن الكبير في نسب البقاء يعكس التقدم العلاجي غير المسبوق في هذا المجال.
خاتمة — رسالة لكل من يواجه هذا التحدي
اللوكيميا ليست نهاية القصة. هي فصل صعب، نعم، لكن الطب الحديث أعطى الأطباء والمرضى أسلحة لم تكن موجودة قبل سنوات قليلة: علاجات موجّهة تُهاجم الخلية السرطانية بدقة الليزر، وعلاجات مناعية تُعلّم جسمك كيف يُقاتل بنفسه، وزراعات خلايا جذعية تُعيد بناء النظام من الصفر. الأرقام لا تكذب: نسب الشفاء ترتفع عاماً بعد عام. الكشف المبكر والالتزام بالخطة العلاجية والمتابعة الدقيقة — هذا الثالوث هو ما يصنع الفرق بين الخوف والأمل الحقيقي.
إلى كل مريض وكل أسرة تقرأ هذه الكلمات: لستم وحدكم. أنتم أقوى مما تظنون، والعلم يقف إلى جانبكم. لا تدعوا الخوف من المجهول يسرق منكم خطوة أولى نحو العلاج. وإذا كان هناك شخص في حياتك تأخّر عن زيارة الطبيب رغم ظهور أعراض مقلقة، فكن أنت الصديق الذي يأخذ بيده إلى الفحص — فتحليل دم واحد قد يُغيّر كل شيء.
هل أجريت تحليل دم شاملاً (CBC) خلال العام الأخير؟ إن لم تفعل، فاجعل هذا هو قرارك اليوم.
هل اللوكيميا مرض قاتل لا شفاء منه؟
كم تستغرق مدة علاج ابيضاض الدم عند الأطفال؟
هل يمكن أن يتحوّل ابيضاض الدم المزمن إلى حاد؟
هل يمكن التوقف عن دواء إيماتينيب بعد الشفاء؟
هل تؤثر اللوكيميا على الخصوبة؟
ما الفرق بين زراعة نخاع العظم الذاتية والخيفية؟
هل العلاج الكيميائي يُسبّب العقم بشكل دائم؟
هل يمكن الكشف عن اللوكيميا قبل ظهور الأعراض؟
هل يمكن ممارسة الرياضة أثناء علاج اللوكيميا؟
ما الفرق بين اللوكيميا واللمفوما؟
- تعتمد مقالات موقع وصفة طبية على مراجع علمية محكّمة من مجلات طبية دولية معتمدة.
- يخضع كل محتوى لمراجعة طبية دقيقة من قِبل أطباء متخصصين ومؤهّلين قبل نشره.
- يُحدَّث المحتوى بصفة دورية ليعكس أحدث التوصيات والبروتوكولات الطبية المعتمدة.
- تُوثَّق المصادر والمراجع العلمية بروابطها المباشرة في نهاية كل مقال للتحقق المستقل.
- لا يُشكّل أي محتوى منشور ترويجاً لعلاج بعينه أو تأييداً لمنتج دوائي محدد.
يستند هذا المقال إلى أحدث البروتوكولات والإرشادات الطبية الدولية، وأبرزها:
- European LeukemiaNet (ELN) 2022: توصيات تشخيص وعلاج AML وCML.
- Children’s Oncology Group (COG) 2024: بروتوكولات علاج ALL عند الأطفال.
- American Society of Hematology (ASH) 2024: إرشادات علاج CLL وCML.
- National Comprehensive Cancer Network (NCCN) 2025: الإرشادات الشاملة لسرطانات الدم.
- وزارة الصحة السعودية — برنامج الأورام الوطني: البروتوكولات المعتمدة محلياً.
- وزارة الصحة الإماراتية — الدليل الإكلينيكي لسرطانات الدم 2024.
- FDA Drug Approvals 2017-2025: قائمة الأدوية الموجّهة المعتمدة حديثاً.
المصادر والمراجع
الدراسات والأوراق البحثية
- DiNardo, C. D., Jonas, B. A., Pullarkat, V., et al. (2020). Azacitidine and Venetoclax in Previously Untreated Acute Myeloid Leukemia. New England Journal of Medicine, 383(7), 617–629. DOI: 10.1056/NEJMoa2012971
— دراسة VIALE-A التي أثبتت فعالية فينيتوكلاكس مع أزاسيتيدين في AML عند كبار السن. - Maude, S. L., Laetsch, T. W., Buechner, J., et al. (2018). Tisagenlecleucel in Children and Young Adults with B-Cell Lymphoblastic Leukemia. New England Journal of Medicine, 378(5), 439–448. DOI: 10.1056/NEJMoa1709866
— الدراسة المحورية لعلاج CAR-T (كيمريا) في ALL عند الأطفال والشباب. - Hochhaus, A., Baccarani, M., Silver, R. T., et al. (2020). European LeukemiaNet 2020 recommendations for treating chronic myeloid leukemia. Leukemia, 34(4), 966–984. DOI: 10.1038/s41375-020-0776-2
— توصيات الشبكة الأوروبية لسرطان الدم لعلاج CML بمثبطات TKI. - Döhner, H., Wei, A. H., Appelbaum, F. R., et al. (2022). Diagnosis and Management of AML in Adults: 2022 ELN Recommendations. Blood, 140(12), 1345–1377. DOI: 10.1182/blood.2022016867
— أحدث توصيات الشبكة الأوروبية لتشخيص وعلاج AML. - Hunger, S. P., & Mullighan, C. G. (2015). Acute Lymphoblastic Leukemia in Children. New England Journal of Medicine, 373(16), 1541–1552. DOI: 10.1056/NEJMra1400972
— مراجعة شاملة لبيولوجيا وعلاج ALL عند الأطفال. - Hallek, M., Al-Sawaf, O. (2021). Chronic lymphocytic leukemia: 2022 update on diagnostic and therapeutic procedures. American Journal of Hematology, 97(S1), S3–S12. DOI: 10.1002/ajh.26367
— تحديث لبروتوكولات تشخيص وعلاج CLL.
الجهات الرسمية والمنظمات
- American Cancer Society (2024). Leukemia: Types, Symptoms, and Treatment.
— ملخص شامل وحديث عن أنواع اللوكيميا وعلاجها. - National Cancer Institute (NCI). Leukemia — Patient Version.
— معلومات موثوقة للمرضى من المعهد الوطني للسرطان الأميركي. - World Health Organization (WHO) — IARC. Global Cancer Observatory.
— إحصاءات عالمية عن الإصابة بسرطانات الدم. - U.S. Food and Drug Administration (FDA). Approved Drugs for Leukemia.
— قائمة الأدوية المعتمدة حديثاً لعلاج اللوكيميا. - Leukemia & Lymphoma Society (LLS). Facts and Statistics.
— إحصاءات وحقائق من أكبر منظمة خيرية مختصة بسرطانات الدم.
الكتب والموسوعات العلمية
- Hoffbrand, A. V., Pettit, J. E., & Vyas, P. (2019). Hoffbrand’s Essential Haematology, 8th Edition. Wiley-Blackwell.
— مرجع أكاديمي أساسي في أمراض الدم يشمل فصولاً تفصيلية عن اللوكيميا. - DeVita, V. T., Lawrence, T. S., & Rosenberg, S. A. (2023). DeVita, Hellman, and Rosenberg’s Cancer: Principles & Practice of Oncology, 12th Edition. Wolters Kluwer.
— الموسوعة الأشمل في علم الأورام وبروتوكولات العلاج. - Kaushansky, K., et al. (2021). Williams Hematology, 10th Edition. McGraw-Hill.
— المرجع الذهبي في أمراض الدم للأطباء والباحثين.
مقالات علمية مبسّطة
- Scientific American (2023). How CAR-T Cell Therapy Is Transforming Cancer Treatment.
— مقالة مبسّطة عن تأثير علاج CAR-T في تحويل مسار علاج سرطانات الدم.
قراءات إضافية ومصادر للتوسع
- Swerdlow, S. H., et al. (2017). WHO Classification of Tumours of Haematopoietic and Lymphoid Tissues, Revised 4th Edition. IARC Press.
— لماذا نقترح عليك قراءته؟ هذا الكتاب هو المرجع الدولي المعتمد لتصنيف سرطانات الدم. يضم معايير التشخيص المجهري والجيني لكل نوع من أنواع اللوكيميا. ضروري لأي طالب أو باحث يريد فهم التصنيفات بعمق. - Pui, C. H. (2019). Precision medicine in acute lymphoblastic leukemia. Frontiers in Medicine.
— لماذا نقترح عليك قراءته؟ يُقدّم رؤية مستقبلية عن كيف سيُصبح علاج ALL مخصّصاً لكل مريض بناءً على بصمته الجينية الفردية — وهو الاتجاه البحثي الأبرز حالياً. - Shlush, L. I. (2018). Age-related clonal hematopoiesis. Blood, 131(5), 496–504.
— لماذا نقترح عليك قراءته؟ يشرح ظاهرة “التكاثر النسيلي المرتبط بالعمر” (CHIP) التي تُمثّل المرحلة ما قبل السرطانية وكيف قد تتحوّل بعض الطفرات المرتبطة بالشيخوخة إلى لوكيميا. موضوع متقدّم ومثير.
إذا ساعدك هذا المقال أو أجاب عن سؤال كان يؤرقك، فشاركه مع من يحتاجه. المعرفة الطبية الصحيحة قد تُنقذ حياة. وإذا كانت لديك أعراض مقلقة أو شُخّص أحد أحبائك حديثاً، فلا تتردد — الخطوة الأولى دائماً هي زيارة اختصاصي أمراض الدم. أنت لا تواجه هذا وحدك.
المحتوى المنشور في موقع وصفة طبية معدٌّ لأغراض التثقيف الصحي والإعلامي العام فحسب، ولا يُمثّل بديلاً عن الاستشارة الطبية المتخصصة أو التشخيص الطبي أو العلاج.
لا ينبغي الاعتماد على هذه المعلومات لاتخاذ قرارات علاجية أو تغيير أي دواء أو جرعة دون الرجوع إلى طبيب مؤهّل ومختص. كل حالة طبية فردية وتحتاج إلى تقييم شخصي دقيق.
في حالات الطوارئ الطبية، توجّه فوراً إلى أقرب مرفق صحي أو اتصل بالإسعاف. موقع وصفة طبية لا يتحمّل أي مسؤولية قانونية أو طبية ناجمة عن تطبيق المعلومات المنشورة دون استشارة طبية متخصصة.
د. سوزان عبد الحميد السعدي — استشارية أمراض الدم وزرع الخلايا الجذعية