انحلال الدم الوليدي: الأسباب، الأعراض، وخطوات العلاج والوقاية
كيف يتحول اختلاف فصيلة الدم بين الأم والجنين إلى خطر حقيقي على حياته؟

انحلال الدم الوليدي (Hemolytic Disease of the Newborn – HDN) حالة مناعية خطيرة يُهاجم فيها جهاز مناعة الأم كريات الدم الحمراء الخاصة بجنينها عبر أجسام مضادة تعبر المشيمة. يؤدي ذلك إلى تكسّر هذه الكريات وارتفاع البيليروبين (Bilirubin) وفقر الدم الجنيني. تصيب هذه الحالة نحو 3 إلى 80 من كل 100,000 ولادة حية وفقاً لشدة النوع المسبِّب، ويمكن الوقاية منها بنسبة تتجاوز 99% حين تُتَّبع البروتوكولات الحديثة.
أبرز ما ستتعلمينه في هذا المقال — اقرئيه في أقل من دقيقة
✅ الحلول والإجراءات الفورية
- اعرفي فصيلة دمكِ وعامل Rh من أول زيارة للطبيب — سؤال واحد قد ينقذ حياة جنينكِ.
- إذا كنتِ Rh-سالبة: تلقّي حقنة Anti-D في الأسبوع 28 وخلال 72 ساعة بعد كل ولادة أو إجهاض.
- اليرقان الذي يظهر قبل 24 ساعة من الولادة ليس طبيعياً — توجّهي للمستشفى فوراً.
🔬 الحقائق العلمية الجوهرية
- الأجسام المضادة IgG تعبر المشيمة وتهاجم كريات دم الجنين مسببةً فقر الدم واليرقان.
- تعارض Rh أشد خطورة ويزداد مع كل حمل — تعارض ABO أكثر شيوعاً وأخف وطأة.
- قياس سرعة الشريان الدماغي الأوسط (MCA-PSV) بالدوبلر يكشف فقر الدم الجنيني بلا إبرة.
- نقل الدم داخل الرحم يُنقذ أكثر من 94% من الأجنة المصابة في المراكز المتخصصة.
⚠️ تحذير طبي لا تتجاهليه
📋 خطوات تطبيقية
- قبل الحمل: احفظي فصيلتكِ وفصيلة زوجكِ.
- الأسبوع 28: لا تفوّتي حقنة Anti-D إذا كنتِ Rh-سالبة.
- بعد الولادة: اطلبي فحص كومبس المباشر من دم الحبل السري.
- في الشهرين الأولين: فحوصات دم دورية للكشف عن فقر الدم المتأخر.
تنبيه صحي: المعلومات الواردة في هذا المقال هي للتثقيف الصحي فقط ولا تُغني بأي حال عن استشارة الطبيب المختص.
هل أخبركِ طبيبكِ أن فصيلة دمكِ سالبة بينما فصيلة زوجكِ موجبة، ثم تركتِ العيادة وأنتِ تحملين في صدركِ قلقاً غامضاً لا تعرفين حدوده؟ أو ربما سمعتِ من صديقة أن طفلها أُدخل الحضّانة فور ولادته بسبب “اليرقان الشديد” ولم تفهمي السبب الحقيقي. هذا المقال كُتب خصيصى لكِ: سنمشي معاً خطوة بخطوة داخل هذه الحالة الطبية، نفهمها من جذورها، ونضع بين يديكِ كل ما تحتاجينه لتحمي طفلكِ قبل أن يُولد وبعد أن يصل إلى حضنكِ.
تخيّلي هذا المشهد: سارة، أم سعودية في حملها الثاني، فصيلة دمها O سالب (O-) وفصيلة زوجها A موجب (A+). في حملها الأول لم تحدث أي مشكلة وأنجبت طفلاً سليماً. لكنها لم تتلقَّ حقنة الغلوبولين المناعي (Anti-D Immunoglobulin) بعد الولادة الأولى. في حملها الثاني، بدأ جسمها يُنتج أجساماً مضادة تعبر المشيمة وتهاجم كريات دم جنينها. عند الأسبوع 30 لاحظ طبيبها عبر الموجات فوق الصوتية تجمّع سوائل حول قلب الجنين. التشخيص: انحلال الدم الوليدي من نوع Rh. لو أن سارة تلقّت تلك الحقنة في وقتها، لما وصل الأمر إلى هذا الحد. الخلاصة العملية: اسألي طبيبكِ عن فصيلة دمكِ وعامل Rh في أول زيارة متابعة حمل — هذا السؤال البسيط قد ينقذ حياة طفلكِ.
اقرأ أيضاً: الفحوصات الطبية الدورية: متى يجب أن تبدأ وما الذي تحتاجه في كل عمر؟
ما هو انحلال الدم الوليدي (HDN) وكيف يحدث داخل الرحم؟
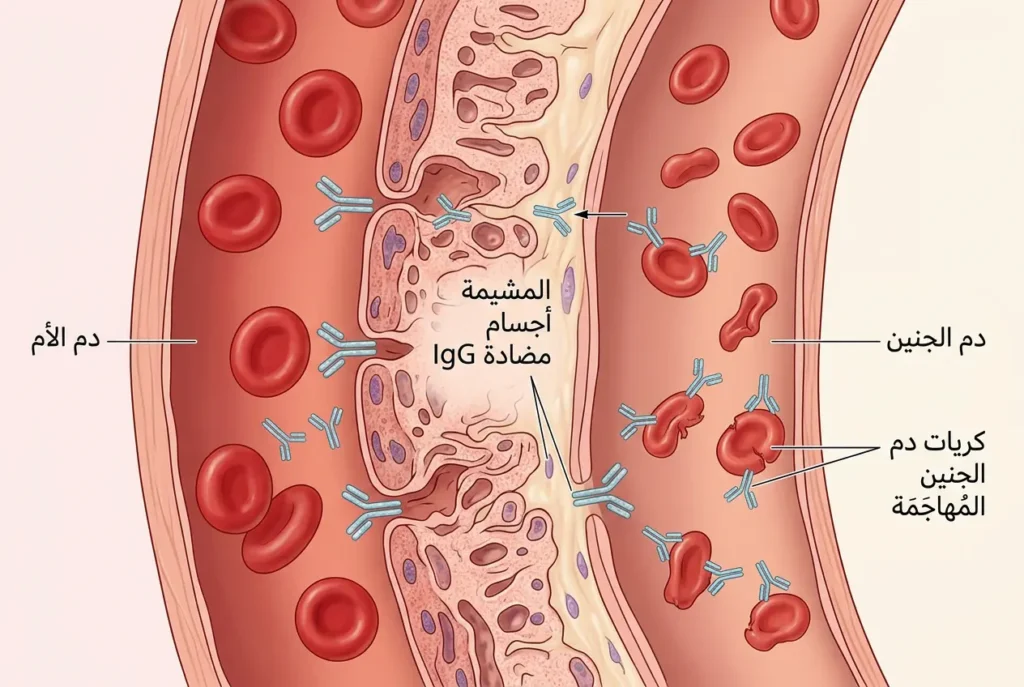
لفهم هذه الحالة، تخيّلي أن جسمكِ يملك جيشاً من الحراس — هم خلايا جهاز المناعة — مهمتهم حماية جسمكِ من أي جسم غريب يدخل إليه. في الوضع الطبيعي، يتعرّف هذا الجيش على الجنين بوصفه “جزءاً منكِ” بفضل آليات مناعية معقدة تمنع الرفض. لكن حين تختلف فصيلة دم الجنين عن فصيلة دمكِ في مستضدات معيّنة (Antigens) موجودة على سطح كريات دمه الحمراء — وخصوصاً مستضد D الخاص بعامل Rh أو مستضدات نظام ABO — فإن جهازكِ المناعي قد يتعامل مع كريات دم الجنين كأنها “غزاة” يجب تدميرهم.
العملية تسير على النحو التالي: في لحظة ما خلال الحمل أو الولادة، تتسرّب كمية صغيرة من دم الجنين إلى مجرى دم الأم عبر المشيمة. إذا كانت كريات دم الجنين تحمل مستضداً لا يملكه جسم الأم، يبدأ جهاز مناعتها بإنتاج أجسام مضادة (Antibodies) موجّهة ضد هذا المستضد. هذه الأجسام المضادة — وتحديداً من نوع IgG — صغيرة بما يكفي لتعبر المشيمة بسهولة وتصل إلى الجنين. هناك، ترتبط بسطح كريات دمه الحمراء وتُعلّمها للتدمير. فيقوم طحال الجنين وكبده بتحطيم هذه الكريات المُعلَّمة بمعدل يتجاوز قدرة نخاع عظمه على تعويضها. النتيجة: فقر دم متصاعد، وتراكم مادة البيليروبين الناتجة عن تكسّر الكريات، وسلسلة من المضاعفات قد تصل — في الحالات الشديدة — إلى فشل القلب الجنيني.
لماذا يُعَدُّ فهم الفرق بين تعارض Rh وتعارض ABO نقطة الانطلاق الأولى؟
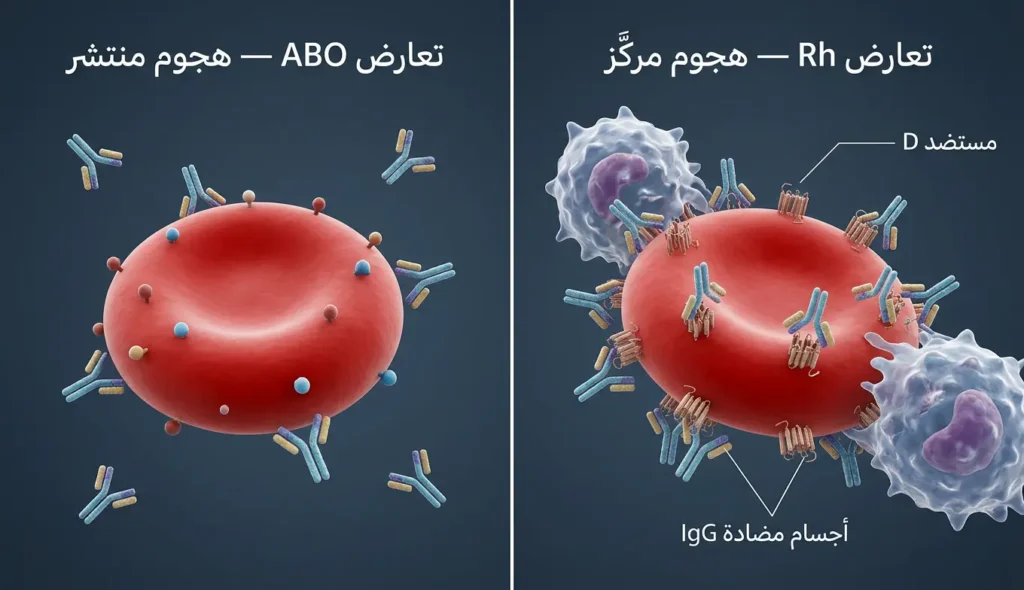
هنا النقطة التي تغيب عن كثير من المقالات المنافسة، وهي التمييز الدقيق بين نوعين مختلفين تماماً في شدتهما رغم أنهما يقعان تحت مظلة انحلال الدم الوليدي.
عدم تطابق العامل الريسوسي (Rh Incompatibility): الأشد خطورة
يحدث حين تكون الأم سالبة العامل الريسوسي (Rh-negative) والجنين موجباً (Rh-positive) — أي أنه ورث مستضد D من أبيه. في الحمل الأول، نادراً ما تظهر مشكلة واضحة؛ إذ إنَّ التعرض الأول عادةً لا يُنتج سوى أجسام مضادة من نوع IgM الكبيرة التي لا تعبر المشيمة بسهولة. لكن المشكلة الحقيقية تبدأ في الأحمال التالية. فقد أصبح جهاز مناعة الأم “يتذكّر” مستضد D، وعند أي تعرّض جديد — ولو بقطرة دم ضئيلة من الجنين الثاني — يطلق استجابة مناعية ثانوية سريعة وعنيفة تُنتج كميات هائلة من IgG المدمّر. هذا ما يجعل مرض الريسوس يزداد شدة مع كل حمل لاحق إذا لم تُتخذ إجراءات وقائية.
حقيقة طبية: قبل اكتشاف حقنة Anti-D عام 1968، كان انحلال الدم الوليدي الناتج عن تعارض Rh يقتل نحو 10,000 طفل سنوياً في الولايات المتحدة وحدها. اليوم انخفض هذا الرقم بأكثر من 95% بفضل برامج الوقاية المنهجية.
عدم تطابق فصائل الدم ABO: الأكثر شيوعاً والأقل خطورة
هذا النوع يحدث غالباً حين تكون الأم فصيلتها O والجنين فصيلته A أو B. السبب أن أصحاب الفصيلة O يملكون طبيعياً أجساماً مضادة (Anti-A وAnti-B) في دمهم. لكن لماذا يكون أخفّ وطأة من تعارض Rh؟ لأن مستضدات A وB لا تقتصر على كريات الدم الحمراء فحسب، بل توجد أيضاً على أسطح خلايا كثيرة في جسم الجنين وفي السائل الأمنيوسي، ما يعني أن الأجسام المضادة “تتشتت” ولا تتركّز كلها على مهاجمة الكريات الحمراء. كما أن مستضدات ABO على سطح كريات الدم الوليدية لم تنضج بالكامل بعد، فتكون أقل قابلية للارتباط بالأجسام المضادة. ومع ذلك، لا ينبغي الاستهانة بهذا النوع؛ إذ إنَّه قد يسبب يرقاناً مرضياً يستدعي علاجاً ضوئياً مكثفاً خلال الساعات الأولى بعد الولادة.
بالمقابل، يختلف عدم تطابق فصائل الدم ABO عن مرض الريسوس في نقطة جوهرية: يمكن أن يظهر من الحمل الأول، لأن الأجسام المضادة Anti-A وAnti-B موجودة سلفاً في دم الأم من فصيلة O دون الحاجة لتحسس سابق.
اقرأ أيضاً: اليرقان الوليدي (صفار المواليد): الأسباب، درجات الخطورة، وخطوات العلاج الطبية
| وجه المقارنة | تعارض Rh | تعارض ABO |
|---|---|---|
| الشيوع النسبي | أقل شيوعاً | الأكثر شيوعاً |
| الشدة السريرية | الأشد خطورة | أخف وطأة في الغالب |
| الحمل المتأثر | نادراً الأول، يزداد في الأحمال التالية | يمكن أن يظهر من الحمل الأول |
| نوع الجسم المضاد المسبِّب | IgG (يعبر المشيمة) | IgG وIgM (IgM لا يعبر المشيمة) |
| هدف الهجوم المناعي | مستضد D على كريات الجنين فقط | مستضدات A/B متشتتة على خلايا متعددة |
| الحاجة لتحسس سابق | نعم، ضرورة تعرض سابق لمستضد D | لا، الأجسام المضادة موجودة طبيعياً |
| احتمالية موه الجنين | مرتفعة في الحالات غير المُعالجة | نادرة جداً |
| الوقاية المتاحة | حقنة Anti-D فعّالة جداً (>99%) | لا توجد وقاية دوائية محددة |
| فحص كومبس المباشر للمولود | إيجابي بقوة | إيجابي ضعيف أو سلبي أحياناً |
| استجابة للعلاج الضوئي | جيدة مع IVIG في الحالات الشديدة | جيدة في معظم الحالات |
الأجسام المضادة النادرة الأخرى
لا يقتصر داء الانحلال الدموي عند الجنين على Rh وABO. هناك مستضدات أخرى أقل شهرة لكنها قد تسبب انحلالاً شديداً، مثل مستضدات Kell وDuffy وKidd وMNS. مستضد Kell تحديداً يستحق الإشارة لأنه لا يكتفي بتدمير كريات الدم الحمراء الناضجة، بل يهاجم أيضاً الخلايا السليفة في نخاع عظم الجنين (Erythroid precursors)، ما يعني أنه يُعطّل إنتاج الكريات الجديدة أصلاً — وهذا يجعل فقر الدم أشد وأصعب تعويضاً.
معلومة سريعة: تمثّل الأجسام المضادة لمستضد Kell ثالث أشيع سبب لانحلال الدم الوليدي بعد Rh وABO، وتُكتشف عادةً عبر فحص الأجسام المضادة الروتيني في الثلث الأول من الحمل.
متى يدق ناقوس الخطر ومن هي الأم الأكثر عرضة؟
ليست كل أم سالبة العامل الريسوسي ستُصاب بالتحسس، وليست كل حالة اختلاف زمرة الدم بين الأم والجنين ستنتهي بمشكلة. لكن هناك عوامل محددة ترفع احتمالية تكوين الأجسام المضادة بصورة كبيرة. فما هي هذه العوامل؟
العامل الأول والأهم هو الأحمال المتعددة السابقة دون تلقّي حقنة Anti-D. كل ولادة سابقة لطفل Rh-positive تمثل فرصة تعرّض جديدة، وكل تعرّض يُعمّق “الذاكرة المناعية” ويجعل الاستجابة أعنف في المرة التالية. العامل الثاني هو الإجهاض — سواء كان تلقائياً أو مُتعمَّداً — لأن أنسجة الحمل المفقود قد تحمل مستضد D وتتسرب إلى دم الأم. كثير من النساء لا يعرفن أن الإجهاض في الأسبوع الثامن أو العاشر يمكن أن يُحدث تحسساً كافياً لإيذاء الجنين التالي.
الحمل خارج الرحم (Ectopic pregnancy) يمثل عامل خطر آخر يُغفل كثيراً. كذلك الحال مع الإجراءات الغازية في أثناء الحمل مثل بزل السائل الأمنيوسي (Amniocentesis) أو أخذ عينة من الزغابات المشيمية (Chorionic villus sampling – CVS)، لأن هذه الإجراءات قد تسبب نزفاً جنينياً-أمومياً مجهرياً (Fetomaternal hemorrhage). الجدير بالذكر أن التعرّض لرضوض في البطن — حتى لو بدت بسيطة كحادث سير خفيف أو سقوط — قد يدفع كمية من دم الجنين عبر المشيمة إلى دوران الأم.
نقل الدم الخاطئ يُعَدُّ سبباً نادراً لكنه مدمّر. إذا تلقّت امرأة Rh-negative وحدة دم Rh-positive عن طريق الخطأ في أي مرحلة من حياتها — حتى قبل سنوات من الحمل — فإن جسمها قد يكون قد تحسّس بالفعل، وستبدأ المشكلة من الحمل الأول.
نقطة تستحق الانتباه: في المملكة العربية السعودية، تبلغ نسبة السكان ذوي العامل الريسوسي السالب نحو 8-10%، وهي نسبة مشابهة للمتوسط العالمي. هذا يعني أن عشرات الآلاف من الحوامل سنوياً في المملكة بحاجة لفحص التحسس ومتابعة دقيقة.
اقرأ أيضاً: حاسبة موعد الولادة المتوقع
ما الأعراض التحذيرية التي يجب ألا تتجاهلها الأم أو الطبيب؟
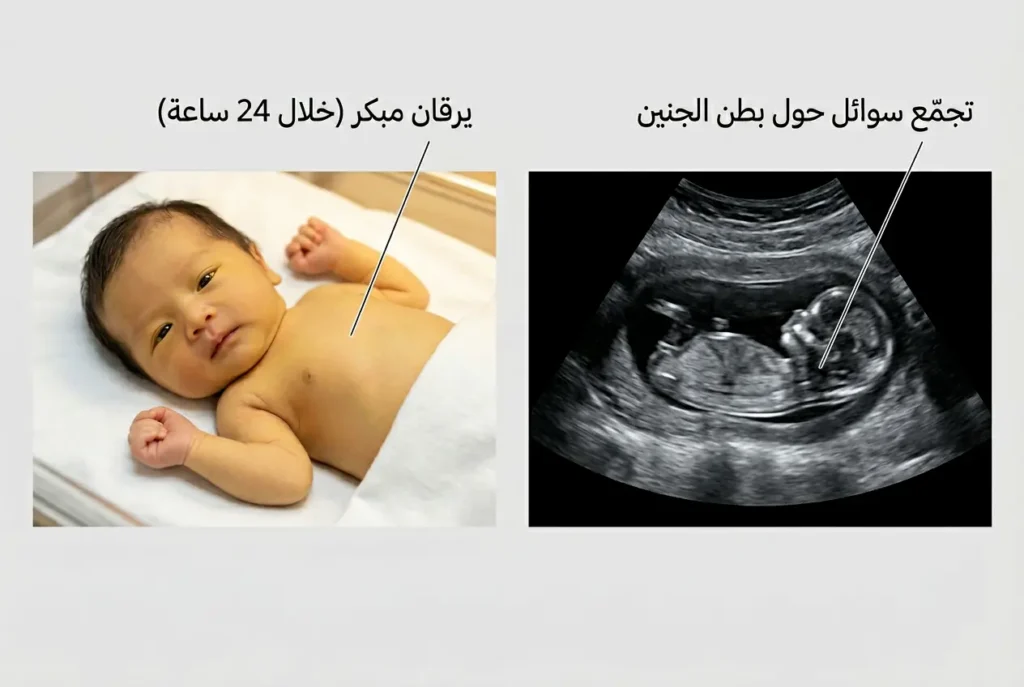
الخطورة في انحلال الدم الوليدي أن أعراضه قد تكون صامتة تماماً في بدايتها — الأم لا تشعر بأي ألم أو تغيّر، بينما جنينها يعاني من تكسّر كرياته بهدوء خلف جدار الرحم. لذلك فإن المتابعة الطبية المنتظمة ليست رفاهية بل ضرورة إنقاذية.
الأعراض في أثناء وجود الجنين في الرحم
لا تستطيع الأم اكتشاف هذه الأعراض بنفسها؛ الطبيب هو من يكتشفها عبر الموجات فوق الصوتية. أبرز ما يبحث عنه الطبيب هو موه الجنين الشامل (Hydrops fetalis) — حالة تتراكم فيها السوائل في تجاويف جسم الجنين (حول القلب، والرئتين، والبطن، وتحت الجلد). تخيّلي أن جسم الجنين يتحوّل إلى إسفنجة مشبعة بالماء لأن قلبه الصغير لم يعد قادراً على ضخ الدم بكفاءة بسبب فقر الدم الشديد. يظهر أيضاً تضخّم في كبد الجنين وطحاله (Hepatosplenomegaly) لأنهما يعملان بأقصى طاقتهما لمحاولة إنتاج كريات دم جديدة تعويضاً عن المدمّرة — وهو ما يُسمى “التكوّن الدموي خارج النخاع” (Extramedullary hematopoiesis). قد يلاحظ الطبيب أيضاً زيادة سماكة المشيمة أو كثافة السائل الأمنيوسي.
الأعراض بعد الولادة مباشرة
هنا تظهر العلامات على المولود بوضوح. العلامة الأولى والأكثر إنذاراً هي اليرقان المبكر — اصفرار الجلد والعينين خلال أول 24 ساعة من الحياة. في الوضع الطبيعي، يظهر اليرقان الفسيولوجي (الطبيعي) عند حديثي الولادة بعد 48-72 ساعة ويكون خفيفاً. لكن حين يظهر اليرقان خلال الساعات الأولى، فهذا جرس إنذار قوي يشير إلى يرقان حديثي الولادة المرضي الناتج عن تكسّر سريع في الكريات.
على النقيض من ذلك، قد يكون الشحوب الشديد هو العلامة السائدة بدلاً من الاصفرار — خاصة في الحالات التي يكون فيها فقر الدم هو المشكلة الأساسة أكثر من ارتفاع البيليروبين. صعوبة التنفس، وضعف الرضاعة، والخمول الشديد، وتسارع نبضات القلب — كلها علامات تكشف أن جسم المولود يكافح للتعويض عن نقص حاد في خلايا الدم الحمراء الحاملة للأكسجين.
هل تعلم؟ يستطيع جسم المولود السليم تحمّل مستويات بيليروبين تصل إلى 12-15 ملغ/دل دون ضرر. لكن في انحلال الدم الوليدي، قد يقفز هذا المستوى إلى 20 أو 25 ملغ/دل خلال ساعات قليلة — وهو مستوى كافٍ لإلحاق ضرر دماغي دائم إذا لم يُعالج فوراً.
اقرأ أيضاً: لماذا تشعر بالتعب المستمر رغم النوم الكافي؟ الأسباب المخفية والحلول الفعالة
ماذا يحدث فعلاً حين يتأخر التشخيص أو العلاج؟
الحديث عن المضاعفات ليس هدفه التخويف، بل بيان أهمية التدخل المبكر. المعرفة هنا سلاح.
أخطر مضاعفات ارتفاع البيليروبين غير المباشر (Unconjugated bilirubin) هو ما يُعرف باليرقان النووي (Kernicterus). اسمه مشتق من كلمة ألمانية تعني “نواة صفراء”، لأن البيليروبين يترسّب حرفياً في نوى الدماغ العميقة — تحديداً في العقد القاعدية (Basal ganglia) وجذع الدماغ — ويسبب تلفاً عصبياً لا رجعة فيه. الطفل الذي يصاب باليرقان النووي قد يعاني من شلل دماغي (Cerebral palsy)، وفقدان سمع عصبي حسي (Sensorineural hearing loss)، وشلل في حركة العينين للأعلى، وتأخر ذهني شديد. هذا الكابوس يمكن تجنبه بالكامل بالعلاج الضوئي أو تبديل الدم في الوقت المناسب.
فقر الدم الشديد غير المُعالَج يدفع قلب الجنين للعمل بجهد مضاعف لتعويض نقص الأكسجين، ما يؤدي إلى قصور القلب الاحتقاني الجنيني (Fetal congestive heart failure). هذا القصور هو الذي ينتهي بموه الجنين الشامل — وهو آخر محطة قبل الوفاة داخل الرحم (Intrauterine fetal death) إذا لم يُتدخّل. كما أن تلف خلايا الكبد الجنيني نتيجة التكوّن الدموي المفرط قد يسبب نقص بروتين الألبومين (Hypoalbuminemia)، ما يزيد تسرب السوائل إلى الأنسجة ويفاقم الاستسقاء.
لقد أكدت دراسة نُشرت في مجلة Blood عام 2021 أن التدخل المبكر بنقل الدم داخل الرحم في حالات فقر الدم الجنيني الشديد رفع معدل البقاء على قيد الحياة إلى أكثر من 90%، مقارنة بأقل من 50% في الحالات التي لم تتلقَّ تدخلاً.
| وجه المقارنة | ✔ التدخل المبكر | ✘ التأخر في التشخيص أو العلاج |
|---|---|---|
| مآل فقر الدم الجنيني | تصحيح بنقل دم داخل الرحم (IUT) بمعدل بقاء >94% | تفاقم حتى قصور قلب جنيني وموه جنيني شامل |
| مستوى البيليروبين عند الولادة | يُراقَب ويُعالَج قبل بلوغ المستويات الحرجة | قد يبلغ 20-25 ملغ/دل خلال ساعات — خطر دماغي مباشر |
| خطر اليرقان النووي (Kernicterus) | شبه معدوم مع بروتوكولات AAP المُطبَّقة | مرتفع — تلف في العقد القاعدية وجذع الدماغ لا يُعكَس |
| الحاجة لتبديل الدم الشامل | نادرة (<5% من الحالات المُدارة مبكراً) | مرتفعة — الملاذ الأخير في حالات البيليروبين الحرج |
| التطور العصبي على المدى البعيد | طبيعي في معظم الأطفال المُعالَجين مبكراً | احتمال شلل دماغي وفقدان سمع وتأخر معرفي |
| وفاة الجنين أو المولود | نادرة جداً في المراكز المتخصصة (<1%) | ما يزال يتسبب في ~14,000 وفاة سنوياً في البلدان منخفضة الدخل |
| التكلفة الإجمالية للعلاج | أقل بكثير — حقنة وقائية + متابعة دورية | مضاعفة — IUT متكررة + حضانة مطوّلة + تأهيل عصبي |
رقم لافت: تُقدّر منظمة الصحة العالمية أن انحلال الدم الوليدي لا يزال يتسبب في وفاة ما يقارب 14,000 حالة وفاة جنينية ووليدية سنوياً في البلدان منخفضة ومتوسطة الدخل، معظمها كان يمكن تجنبه بحقنة Anti-D التي لا يتجاوز ثمنها بضعة دولارات.
المختبر الفسيولوجي — للمهتمين بالتفاصيل العلمية الدقيقة
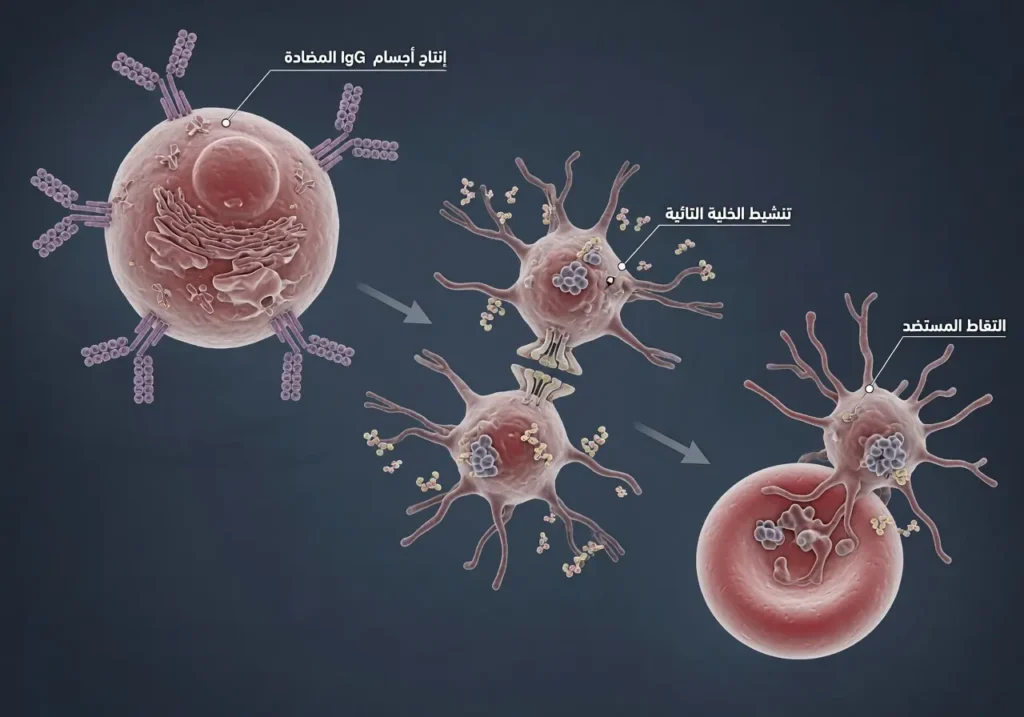
لفهم الآلية الحيوية العميقة لانحلال الدم الوليدي، علينا الغوص إلى المستوى الجزيئي. مستضد D — وهو بروتين عبر غشائي (Transmembrane protein) يُعرف بـ RhD — يتواجد على سطح كريات الدم الحمراء مُرتبطاً ببروتينات RhCE وRhAG ضمن مُعقّد بروتيني (Protein complex) في الغشاء الخلوي. حين تتسرب كريات دم جنينية تحمل RhD إلى دوران الأم السالبة، تلتقطها الخلايا المقدِّمة للمستضد (Antigen-presenting cells – APCs) — وأبرزها الخلايا المتغصّنة الطحالية (Splenic dendritic cells) — التي تُعالج المستضد وتعرضه على سطحها مرتبطاً بجزيئات التوافق النسيجي من النوع الثاني (MHC class II).
هذا العرض يُنشّط الخلايا التائية المساعدة (CD4+ T-helper cells) عبر مسار إشارات مستقبل الخلية التائية (TCR signaling pathway). الخلايا التائية المنشطة تُحرّر سيتوكينات — أبرزها إنترلوكين-4 (IL-4) وإنترلوكين-21 (IL-21) — توجّه الخلايا البائية (B cells) نحو التمايز إلى خلايا بلازمية (Plasma cells) منتجة للأجسام المضادة. في التعرض الأول، تكون الاستجابة بطيئة وتنتج بالدرجة الأولى IgM (خماسي البنية، لا يعبر المشيمة). لكن مع التعرض المتكرر، يحدث ما يُسمى “التحوّل الصنفي” (Class switching) من IgM إلى IgG — وتحديداً النوعين الفرعيين IgG1 وIgG3 اللذين يتميزان بقدرة عالية على عبور المشيمة عبر مستقبلات FcRn (Neonatal Fc receptor) الموجودة على خلايا الأرومة الغاذية المخلوية (Syncytiotrophoblast).
بمجرد وصول IgG إلى الدوران الجنيني وارتباطه بمستضد RhD على سطح كريات الجنين، يبدأ التدمير عبر آليتين رئيستين: الأولى هي البلعمة المعتمدة على الأجسام المضادة (Antibody-dependent cellular phagocytosis – ADCP)، إذ تتعرف البلاعم الطحالية (Splenic macrophages) على الجزء Fc من الأجسام المضادة المرتبطة بسطح الكريات عبر مستقبلات Fcγ وتبتلعها. الآلية الثانية هي تفعيل جزئي للمتمّمة (Complement system)، خاصة عبر المسار الكلاسيكي (Classical pathway)، رغم أن بروتينات تنظيم المتمّمة على سطح الكريات (مثل CD55 وCD59) تُخفف من هذا المسار عادةً، ما يجعل البلعمة الطحالية هي الآلية المهيمنة. هذا يفسر لماذا يتضخم طحال الجنين بشدة — فهو “ساحة المعركة” الرئيسة.
البيليروبين الناتج عن تكسّر الهيم (Heme) يُنقل عبر الألبومين في دم الجنين. في أثناء الحياة داخل الرحم، تتولّى مشيمة الأم تصفية معظم هذا البيليروبين عبر كبدها هي. لكن بعد الولادة، يُقطع هذا “الشريان النجاة”، ويُصبح كبد المولود الصغير — الذي لم ينضج إنزيم UDP-glucuronosyltransferase فيه بعد — هو المسؤول الوحيد عن تحويل البيليروبين غير المباشر (السام للدماغ) إلى البيليروبين المباشر (القابل للإخراج). هذا العجز الإنزيمي الفسيولوجي هو السبب في أن البيليروبين يرتفع بسرعة صاروخية بعد الولادة في حالات الانحلال الشديد.
كيف يُشخَّص انحلال الدم الوليدي بدقة قبل الولادة وبعدها؟
التشخيص المبكر هو الخطوة الأولى لإنقاذ الجنين. ينقسم إلى مرحلتين زمنيتين واضحتين.
الفحوصات قبل الولادة
أول إجراء يُطلب من كل حامل في الزيارة الأولى هو تحديد فصيلة دمها وعامل Rh. إذا كانت Rh-negative، يُجرى لها فحص الأجسام المضادة غير المباشر (Indirect Coombs Test أو Indirect Antiglobulin Test – IAT). هذا الفحص يكشف ما إذا كان دم الأم يحتوي بالفعل على أجسام مضادة موجّهة ضد مستضد D أو مستضدات أخرى. إذا كان الفحص سلبياً في الزيارة الأولى، يُعاد في الأسبوع 28 للتأكد. أما إذا كان إيجابياً، فيُحدَّد عيار الأجسام المضادة (Antibody titer)؛ والعيار الحرج الذي يستدعي مراقبة مكثفة يختلف بين المراكز لكنه عادةً يبلغ 1:16 أو أعلى لمستضد D.
الخطوة التالية — وهي من أهم الابتكارات الحديثة — هي قياس سرعة تدفق الدم في الشريان الدماغي الأوسط للجنين (Middle Cerebral Artery Peak Systolic Velocity – MCA-PSV) عبر الدوبلر بالموجات فوق الصوتية. المبدأ بسيط وعبقري: حين يعاني الجنين من فقر دم، يصبح دمه أقل لزوجة (أرقّ)، فيتدفق بسرعة أكبر في شرايينه. قياس هذه السرعة يُعطي تقديراً غير جراحي لشدة فقر الدم الجنيني بدقة عالية، وقد حلّ محل بزل السائل الأمنيوسي الذي كان يُستخدم سابقاً لقياس البيليروبين عبر مخطط ليلي (Liley chart).
هذا وقد أتاحت التقنيات الحديثة إجراء تحديد فصيلة Rh للجنين عبر الحمض النووي الجنيني الحر في دم الأم (Cell-free fetal DNA – cffDNA) — فحص دم بسيط من ذراع الأم يُجرى بعد الأسبوع 10-12 من الحمل. إذا أظهر الفحص أن الجنين Rh-negative مثل أمه، فلا حاجة لحقنة Anti-D ولا لمتابعة مكثفة. هذا الفحص بدأ يُعتمد رسمياً في عدد متزايد من الدول الأوروبية وبدأت بعض المراكز الكبرى في السعودية بتبنّيه.
اقرأ أيضاً: ما هي تقنية كريسبر (CRISPR-Cas9) وكيف تعيد كتابة مستقبل الطب البشري؟
الفحوصات بعد الولادة
فور ولادة الطفل في حالة اشتباه بانحلال الدم الوليدي، يُسحب دم من الحبل السري (Cord blood) ويُجرى عليه:
- فصيلة الدم وعامل Rh للمولود: لتأكيد عدم التطابق.
- فحص كومبس المباشر (Direct Coombs Test – DAT): يكشف ما إذا كانت أجسام مضادة من الأم قد ارتبطت فعلاً بسطح كريات دم المولود. النتيجة الإيجابية تؤكد التشخيص.
- مستوى البيليروبين الكلي والمباشر: لتحديد شدة اليرقان والحاجة للعلاج الفوري.
- تعداد الدم الكامل (CBC): لتقييم مستوى الهيموغلوبين (Hemoglobin) وعدد الخلايا الشبكية (Reticulocytes) — ارتفاع الشبكيات يعكس محاولة نخاع العظم تعويض الكريات المُدمَّرة.
تؤكد الدكتورة نور الهدى القباني — طبيبة نسائية وتوليد وخبيرة الصحة الإنجابية في موقع وصفة طبية: “أطلب من كل حامل في زيارتها الأولى فحص فصيلة الدم وعامل Rh وفحص الأجسام المضادة. لا يستغرق الأمر سوى عينة دم واحدة، لكنه قد يغيّر مسار الحمل بأكمله. المشكلة أن بعض الأمهات يؤجّلن الزيارة الأولى حتى الشهر الرابع أو الخامس، وهذا تأخير قد يكلّف غالياً.”
ما هي بروتوكولات العلاج المتقدمة المتوفرة اليوم؟

العلاج يعتمد على شدة الحالة وعلى توقيت اكتشافها — قبل الولادة أو بعدها. وعليه فإن الخطة العلاجية تتدرّج من التدخلات الأقل إلى الأكثر اجتياحاً.
التدخلات داخل الرحم
حين يُظهر فحص الدوبلر أن سرعة تدفق الدم في الشريان الدماغي الأوسط للجنين تتجاوز 1.5 مضاعف القيمة الوسطية (1.5 MoM) لعمره الحملي — وهو ما يشير إلى فقر دم متوسط إلى شديد — يُقرّر الفريق الطبي إجراء نقل دم داخل الرحم (Intrauterine transfusion – IUT). يتم ذلك عبر إدخال إبرة دقيقة بتوجيه الموجات فوق الصوتية إلى الوريد السري للجنين (Cordocentesis)، ثم نقل كريات دم حمراء مُركّزة ومُغسولة من فصيلة O Rh-negative — وهي فصيلة متوافقة مع أي جنين — مباشرة إلى دوران الجنين. هذا الإجراء — رغم دقته التقنية العالية — آمن نسبياً في المراكز المتخصصة، وقد يُكرَّر كل 2-4 أسابيع حسب شدة الحالة حتى يصل الجنين إلى عمر حملي يسمح بالولادة الآمنة (عادةً الأسبوع 34-37).
فقد أثبتت دراسة كبيرة نُشرت في مجلة The Lancet عام 2023 أن نقل الدم داخل الرحم في مراكز خبيرة يحقق معدل بقاء يتجاوز 94%، حتى في الحالات المصحوبة بموه جنيني مبكر.
علاجات ما بعد الولادة
بعد خروج الطفل إلى العالم، تبدأ معركة جديدة ضد ارتفاع البيليروبين. العلاج الأول والأكثر استخداماً هو العلاج الضوئي (Phototherapy). المبدأ أن الضوء الأزرق بطول موجي محدد (420-490 نانومتر) يخترق جلد المولود ويحوّل جزيئات البيليروبين غير المباشر (الذائبة في الدهون والسامة للدماغ) إلى مركبات ذائبة في الماء (Lumirubin وphotobilirubin) يستطيع الجسم إخراجها عبر الكلى والصفراء دون الحاجة لمعالجتها في الكبد. العلاج الضوئي المكثف (Intensive phototherapy) يستخدم مصادر ضوء متعددة تحيط بالطفل من جميع الجهات لتعظيم مساحة الجلد المعرّضة.
يشدّد الدكتور عبد الرحمن الصباغ — خبير طب الأطفال وحديثي الولادة في موقع وصفة طبية: “العلاج الضوئي ليس مجرد ‘ضوء عادي’ كما تظن بعض الأمهات. إنه أداة طبية دقيقة تتطلب مراقبة مستمرة لمستوى البيليروبين كل 4-6 ساعات، وتعديل شدة الضوء ومدة التعرض. الطفل يجب أن يكون عارياً قدر الإمكان مع حماية عينيه بغطاء خاص، ويحتاج رضاعة متكررة — كل ساعتين — لأن السوائل تساعد على إخراج البيليروبين المُحوَّل.”
الخيار الثاني هو الغلوبولين المناعي الوريدي (Intravenous Immunoglobulin – IVIG). يُعطى للمولود بجرعة 0.5-1 غرام/كغ عبر الوريد خلال ساعتين. آلية عمله أنه يُغرق مستقبلات Fcγ على سطح البلاعم الطحالية بأجسام مضادة “بريئة”، فيمنعها من التعرّف على كريات الدم المُعلَّمة بالأجسام المضادة المدمّرة ويبطئ عملية التكسير. يُستخدم حين يكون البيليروبين يرتفع بسرعة رغم العلاج الضوئي المكثف، أو حين يقترب من مستوى تبديل الدم.
أما الملاذ الأخير في الحالات الأشد خطورة فهو تبديل الدم الشامل (Exchange Transfusion). يُسحب دم المولود بكميات صغيرة (5-20 مل في كل دورة) عبر قثطار في الوريد السري ويُستبدل بدم مانح طازج متوافق. الهدف ثلاثي: إزالة البيليروبين السام، وإزالة الأجسام المضادة للأم من دوران الطفل، وتعويض كريات الدم المُدمَّرة. يُجرى عادةً بتبديل ضعف حجم دم المولود (Double volume exchange = 160-180 مل/كغ). هذا الإجراء ينطوي على مخاطر — مثل اضطرابات الشوارد (Electrolyte imbalances)، ونقص الكالسيوم، وعدم استقرار الدورة الدموية — لذلك لا يُلجأ إليه إلا حين تفشل الخيارات الأخرى أو حين يكون البيليروبين في مستويات خطيرة.
ومضة علمية: في عام 2024، أظهرت نتائج أولية لتجربة سريرية في عدة مراكز أوروبية أن استخدام عقار Emipalumab — وهو جسم مضاد وحيد النسيلة (Monoclonal antibody) — قد يخفض الحاجة لنقل الدم داخل الرحم في بعض حالات تحسس Rh الشديد. البحث لا يزال في مراحله المبكرة لكنه يمثل أفقاً علاجياً واعداً.
اقرأ أيضاً: العلاج المناعي: كيف تبرمج جسمك ليدمر الخلايا السرطانية ذاتياً؟
التفاصيل الدوائية الدقيقة — حقنة Anti-D وIVIG والعلاج الضوئي
⚠️ تحذير: المعلومات الدوائية التالية للتثقيف فقط ولا تُغني عن وصفة الطبيب المعالج. لا تُعدّل أي جرعة أو توقيت من تلقاء نفسك.
| التدخل | المستقبِل | الجرعة | التوقيت | الهدف | أبرز التحذيرات |
|---|---|---|---|---|---|
| حقنة Anti-D | الأم | 300 ميكروغرام IM | الأسبوع 28 + خلال 72 ساعة بعد الولادة | وقاية من التحسس الريسوسي | لا تُعطى بعد تحسس مؤكد — وقائية فقط |
| Anti-D بعد إجهاض مبكر | الأم | 50 – 120 ميكروغرام IM | خلال 72 ساعة من الإجهاض | منع التحسس بعد فقدان الحمل | ضرورية حتى في الإجهاض الطبيعي |
| IVIG للمولود | المولود | 0.5 – 1 غرام / كغ وريدياً | حين يرتفع البيليروبين رغم العلاج الضوئي | إبطاء تكسّر كريات الدم | خطر نادر لالتهاب أمعاء ناخر (NEC) |
| العلاج الضوئي المكثف | المولود | شدة ≥ 30 ميكروواط / سم² / نانومتر | حسب مخططات AAP 2022 (عمر + وزن + عمر حملي) | تحويل البيليروبين إلى مركبات قابلة للإخراج | حماية العينين إلزامية — رضاعة كل ساعتين |
| تبديل الدم الشامل | المولود | 160 – 180 مل / كغ (ضعف حجم الدم) | عند فشل الخيارات السابقة أو البيليروبين الحرج | إزالة البيليروبين والأجسام المضادة وتعويض الكريات | مراقبة مكثفة — خطر اضطراب الشوارد والكالسيوم |
حقنة الغلوبولين المناعي Anti-D (Rho(D) Immune Globulin)
هذه الحقنة هي حجر الزاوية في الوقاية، وليست علاجاً بعد حدوث التحسس. تُعطى للأم وليس للجنين أو المولود.
الجرعة القياسية:
- في الأسبوع 28 من الحمل: 300 ميكروغرام (1500 وحدة دولية) عضلياً (IM) في عضلة الدالية أو الإلية.
- خلال 72 ساعة بعد الولادة: 300 ميكروغرام إذا كان المولود Rh-positive.
- بعد الإجهاض قبل الأسبوع 12: 50-120 ميكروغرام (تختلف حسب البروتوكول المتّبع).
- بعد الإجهاض بعد الأسبوع 12 أو بعد إجراء غازي: 300 ميكروغرام.
- بعد نزيف أو رضة بطنية في أثناء الحمل: 300 ميكروغرام مع إجراء اختبار كلايهاور-بيتكه (Kleihauer-Betke test) لتقدير حجم النزف الجنيني-الأمومي؛ إذا تجاوز 30 مل من الدم الكامل الجنيني، تُضاف جرعات إضافية (10 ميكروغرام لكل مل دم جنيني إضافي).
الآثار الجانبية: ألم موضعي في مكان الحقن (شائع)، حمى خفيفة عابرة، صداع. نادراً: تفاعلات تحسسية. لا يُعطى لامرأة تحسست بالفعل (أي فحص الأجسام المضادة إيجابي)، لأنه لن يُفيد — الهدف وقائي فقط.
تحذيرات خاصة: لا تُعطى الحقنة لامرأة Rh-positive (لا فائدة). ولا تُعطى إذا أظهر فحص cffDNA أن الجنين Rh-negative. يجب تخزينها في الثلاجة (2-8 درجات مئوية) ولا تُجمَّد.
الغلوبولين المناعي الوريدي (IVIG) للمولود
- الجرعة: 0.5-1 غرام/كغ من وزن المولود، تُسرَّب وريدياً خلال 2-4 ساعات.
- يمكن تكرارها: مرة واحدة بعد 12 ساعة إذا استمر البيليروبين في الارتفاع.
- الآثار الجانبية في حديثي الولادة: حمى، قشعريرة، نادراً التهاب أمعاء ناخر (Necrotizing enterocolitis – NEC) — وهو خطر نادر لكنه خطير أشارت إليه بعض الدراسات الحديثة.
- تحذير: يُقرر استخدامه فقط اختصاصي طب حديثي الولادة بناءً على سرعة ارتفاع البيليروبين وشدة التكسر.
العلاج الضوئي
- العلاج الضوئي المكثف: شدة الإشعاع ≥ 30 ميكروواط/سم²/نانومتر، مع تعريض أكبر مساحة ممكنة من جلد المولود.
- مؤشرات البدء: تختلف حسب عمر المولود بالساعات ووزنه وعمره الحملي، وتُحدد وفق مخططات الأكاديمية الأميركية لطب الأطفال (AAP Phototherapy Guidelines 2022).
- مدة العلاج: مستمرة حتى ينخفض البيليروبين إلى مستوى آمن (عادةً 2-3 ملغ/دل تحت عتبة التبديل).
- آثار جانبية: طفح جلدي خفيف، إسهال مائي، ارتفاع طفيف في درجة الحرارة، جفاف (لذلك تُكثَّف الرضاعة). نادراً: متلازمة الطفل البرونزي (Bronze baby syndrome) في حالات ارتفاع البيليروبين المباشر المصاحب.
يؤكد المستشار الدوائي جاسم محمد مراد — خبير الصحة والإمداد الطبي في موقع وصفة طبية: “حقنة Anti-D متوفرة في جميع مستشفيات المملكة العربية السعودية الكبرى وفي معظم مراكز الرعاية الأولية. لا يوجد تعارض دوائي مهم مع أدوية الحمل الشائعة كالحديد وحمض الفوليك والفيتامينات. لكن يجب إبلاغ الطبيب إذا كانت الأم تتناول أي مثبطات مناعية (Immunosuppressants) لأنها قد تؤثر على فعالية الحقنة. كما أنصح بالانتظار أسبوعين على الأقل بعد حقنة Anti-D قبل تلقي أي لقاح حي مُضعَّف مثل لقاح الحصبة أو الحصبة الألمانية، لأن الغلوبولين المناعي قد يُضعف الاستجابة للّقاح.”
اقرأ أيضاً:
- جدول لقاحات الأطفال الروتينية: المواعيد الدقيقة، الآثار الجانبية، وأهم النصائح للأمهات
- مضادات الالتهاب: أنواعها، استخداماتها، والآثار الجانبية
كيف تعمل إستراتيجية الوقاية الذهبية (درع الحماية)؟
هذا هو القسم الأهم في المقال بأكمله، لأن الوقاية من انحلال الدم الوليدي أسهل بكثير من علاجه — وأرخص — وأنجح.
الفكرة العبقرية خلف حقنة Anti-D بسيطة في مبدئها: إذا تسرّبت كريات دم جنينية تحمل مستضد D إلى دم الأم، فإن الحقنة تُغمر هذه الكريات الغريبة بأجسام مضادة Anti-D جاهزة تُدمّرها بسرعة “بصمت” قبل أن يُلاحظها جهاز مناعة الأم ويبدأ بتصنيع أجسامه المضادة الخاصة. تخيّلي أن شخصاً غريباً دخل حيّكِ ليلاً؛ بدلاً من أن يراه حارس الحي ويُطلق الإنذار ويُجنّد كل الجيران (أي الذاكرة المناعية)، يأتي فريق أمن خاص يُبعده بهدوء قبل أن يلاحظه أحد. النتيجة: لا إنذار، لا تجنيد، لا ذاكرة — وكأن شيئاً لم يحدث.
لكن هناك شرط حاسم: التوقيت. يجب أن تُعطى الحقنة قبل أن يبدأ جهاز مناعة الأم بالاستجابة. لهذا السبب يُوصى بها في الأسبوع 28 من الحمل (كإجراء وقائي روتيني)، ثم مرة ثانية خلال 72 ساعة بعد الولادة إذا كان المولود Rh-positive. فكلما طال التأخير بعد 72 ساعة، قلّت فعالية الحقنة — رغم أن بعض الدراسات تشير إلى فائدة جزئية حتى 13 يوماً بعد التعرض.
والسؤال الذي تطرحه كثير من الأمهات: متى تعطى إبرة الفصيلة للحامل بالتحديد؟ الإجابة تشمل كل الحالات التالية:
- الأسبوع 28 من كل حمل: جرعة روتينية وقائية.
- خلال 72 ساعة بعد الولادة: إذا كان المولود Rh-positive.
- بعد أي إجهاض: تلقائي أو مُتعمَّد، في أي عمر حملي.
- بعد الحمل خارج الرحم.
- بعد بزل السائل الأمنيوسي أو أخذ عينة من الزغابات المشيمية.
- بعد أي نزيف مهبلي في أثناء الحمل.
- بعد أي رضة في البطن.
- بعد تدوير الجنين الخارجي (External cephalic version) لتحويله من وضعية المقعدة.
من المثير أن تعرف: الطبيب الأسترالي جيمس هاريسون — الملقّب بـ “الرجل ذو الذراع الذهبية” — تبرع بدمه أكثر من 1,100 مرة على مدى 60 عاماً لأن دمه يحتوي طبيعياً على تركيز عالٍ جداً من أجسام Anti-D المضادة. استُخدم دمه في تصنيع ملايين جرعات حقنة Anti-D في أستراليا، ويُقدَّر أنه ساهم في إنقاذ حياة أكثر من 2.4 مليون طفل.
صندوق اقتباس طبي:
وفقاً لتقرير صادر عن المعاهد الوطنية الأميركية للصحة (NIH) عام 2023: “أدى الاستخدام المنهجي للغلوبولين المناعي Anti-D منذ ستينيات القرن الماضي إلى انخفاض معدل التحسس الريسوسي من 14% إلى أقل من 0.1% لدى النساء Rh-negative في البلدان التي تطبّق برامج وقاية شاملة.”
ما بين الخرافة والحقيقة: معتقدات خاطئة عن اختلاف فصيلة الدم بين الأم والجنين
❌ الخرافة: اختلاف فصيلة دم الزوجين يعني أن كل أطفالهم سيولدون مرضى.
✅ الحقيقة: اختلاف الفصيلة لا يعني حتمية المرض. المشكلة تحدث فقط حين تتحسس الأم — وهو أمر يمكن منعه بحقنة Anti-D. كثير من الأزواج مختلفي الفصيلة ينجبون أطفالاً أصحاء تماماً دون أي مشكلة. المفتاح هو المتابعة الطبية المبكرة.
❌ الخرافة: إذا كان الطفل الأول سليماً، فلا داعي للقلق في الأحمال التالية.
✅ الحقيقة: العكس هو الصحيح تماماً. الخطر يزداد مع كل حمل لاحق إذا لم تُتخذ إجراءات وقائية بعد الحمل الأول. التحسس المناعي يتراكم ويتضاعف مع كل تعرض جديد، وفقاً لما يؤكده المركز الوطني لمعلومات التقنية الحيوية (NCBI).
❌ الخرافة: حقنة Anti-D خطيرة على الجنين وقد تسبب تشوهات.
✅ الحقيقة: حقنة Anti-D تُعطى للأم وليس للجنين. لقد أُثبتت سلامتها عبر أكثر من 50 عاماً من الاستخدام العالمي على ملايين الحوامل. لا توجد أي دراسة موثوقة تربطها بتشوهات خلقية أو أضرار على الجنين.
❌ الخرافة: يرقان حديثي الولادة دائماً طبيعي ولا يحتاج علاجاً.
✅ الحقيقة: اليرقان الفسيولوجي الخفيف الذي يظهر بعد 48-72 ساعة طبيعي فعلاً ويزول وحده. لكن اليرقان الذي يظهر خلال أول 24 ساعة، أو يرتفع بسرعة كبيرة، أو يتجاوز مستويات معيّنة، هو يرقان مرضي قد يكون ناتجاً عن انحلال الدم الوليدي ويحتاج تدخلاً فورياً لمنع تلف الدماغ.
❌ الخرافة: تعريض المولود لأشعة الشمس عبر النافذة يُغني عن العلاج الضوئي في المستشفى.
✅ الحقيقة: ضوء الشمس عبر النوافذ لا يحتوي على الكمية الكافية من الأطوال الموجية العلاجية (420-490 نانومتر) بالشدة المطلوبة. كما يُعرّض المولود لخطر الحروق الشمسية وعدم انتظام الحرارة. العلاج الضوئي الطبي جهاز مُعاير بدقة ولا يمكن استبداله بأشعة الشمس.
هل يمكن أن يشير يرقان حديثي الولادة إلى مشكلات صحية أخرى؟
يرقان حديثي الولادة المرضي ليس دائماً ناتجاً عن اختلاف زمرة الدم بين الأم والجنين. هناك حالات أخرى قد تتداخل في الأعراض وتستدعي التفريق الدقيق.
أولاً: نقص إنزيم الغلوكوز-6-فوسفات ديهيدروجيناز (G6PD Deficiency) — وهو اضطراب وراثي شائع في منطقة الخليج العربي والسعودية تحديداً (تصل نسبته إلى 2-6% من السكان)، يسبب تكسر كريات الدم عند التعرض لمحفّزات معينة مثل بعض الأدوية أو الفول. قد يظهر باليرقان الشديد عند حديثي الولادة ويختلط مع انحلال الدم الوليدي المناعي.
ثانياً: قصور الغدة الدرقية الخلقي (Congenital hypothyroidism) — يُبطئ أيض البيليروبين في الكبد ويسبب يرقاناً مطوّلاً. يُكشف عنه عبر فحص الكعب (Newborn screening) الذي يُجرى روتينياً في مستشفيات المملكة.
ثالثاً: رتق القنوات الصفراوية (Biliary atresia) — حالة نادرة لكنها خطيرة تسبب يرقاناً بارتفاع البيليروبين المباشر (وليس غير المباشر كما في انحلال الدم). التمييز مهم لأن العلاج مختلف تماماً ويتطلب تدخلاً جراحياً مبكراً.
رابعاً: كثرة الكريات الحمراء الكروية الوراثية (Hereditary spherocytosis) — خلل في بنية غشاء كريات الدم يجعلها كروية وهشة وسهلة التكسر. فحص كومبس المباشر يكون سلبياً في هذه الحالة — وهذا ما يميّزها عن انحلال الدم الوليدي المناعي.
اقرأ أيضاً: مرض السكري: ما هو وكيف تتعرف على أعراضه وأسبابه؟
علاج انحلال الدم الوليدي للحوامل والمرضعات: المسموح والممنوع
⚠️ تنبيه طبي: أي قرار علاجي يخص الحامل يجب أن يتم بالتنسيق بين طبيب التوليد وطبيب حديثي الولادة. لا تتناولي أي دواء أو مكمّل دون استشارة طبيبك المتابع.
المسموح والآمن
حقنة Anti-D آمنة تماماً خلال الحمل والرضاعة — لا تؤثر على الجنين ولا تنتقل بكميات ذات شأن في حليب الأم. مكملات الحديد وحمض الفوليك ضرورية للحامل التي تحمل جنيناً معرّضاً لانحلال الدم، لأن جسمها يحتاج لتعويض الأكسجين الذي يُهدر بسبب تكسر كريات الجنين. فيتامين D والكالسيوم آمنان بالجرعات الموصى بها.
الممنوع والمحظور
لا توجد أدوية تتناولها الأم لعلاج انحلال الدم الوليدي بعد حدوث التحسس — العلاج يكون موجهاً للجنين (نقل دم داخل الرحم) أو للمولود (علاج ضوئي/IVIG/تبديل دم). لكن يجب الحذر من بعض المكملات العشبية التي قد تتداخل مع الحالة:
الكركم والكركمين بجرعات عالية (مكملات مركّزة): الكركمين يمتلك خصائص مضادة للصفيحات الدموية، وإذا كانت الحامل معرّضة لنزف جنيني-أمومي (وهو ما قد يزيد التحسس)، فإن المكملات المركزة قد تفاقم المشكلة نظرياً. استخدام الكركم كتوابل في الطبخ آمن ولا يمثل خطراً.
مكملات الثوم المركزة: تمتلك خصائص مميّعة للدم، ويجب تجنبها خاصة في الثلث الأخير من الحمل. الثوم الطازج في الطعام بكميات معقولة لا يمثل مشكلة.
عشبة الجنسنج: قد تؤثر على مستويات السكر وضغط الدم وتتداخل مع بعض أدوية الحمل. لا يُنصح بها للحامل عموماً.
الحلبة بكميات دوائية كبيرة: قد تسبب تقلصات رحمية في الأشهر الأخيرة. في أثناء الرضاعة تُستخدم أحياناً لزيادة إدرار الحليب، لكن بجرعات معتدلة وتحت إشراف طبي.
القاعدة الذهبية: إذا كنتِ حاملاً وفصيلة دمكِ سالبة، فأخبري طبيبكِ بكل مكمّل عشبي أو غذائي تتناولينه. لا تبدئي بتناول أي مكمّل جديد دون مراجعة قائمة أدويتكِ مع الصيدلي السريري.
اقرأ أيضاً: سكري الحمل: الأسباب والأعراض وطرق السيطرة الفعالة لولادة آمنة
ما التكلفة التقريبية لتدخلات انحلال الدم الوليدي؟
التكلفة تختلف بصورة ملحوظة بناءً على نوع التدخل والبلد والمستشفى.
حقنة Anti-D (الوقائية): تتراوح عالمياً بين 50 و200 دولار أميركي. في المملكة العربية السعودية، تُقدَّم مجاناً ضمن خدمات التأمين الصحي ومستشفيات وزارة الصحة والمستشفيات الحكومية. في المستشفيات الخاصة تتراوح بين 200 و500 ريال سعودي.
العلاج الضوئي: يعتمد على مدة الإقامة في الحضّانة. في السعودية، تتراوح تكلفة الإقامة اليومية في حضّانة حديثي الولادة بالمستشفيات الخاصة بين 3,000 و8,000 ريال سعودي تشمل العلاج الضوئي والمراقبة. في المستشفيات الحكومية تُقدَّم مجاناً للمواطنين.
نقل الدم داخل الرحم: إجراء متخصص جداً يتطلب فريقاً خبيراً وتجهيزات متقدمة. عالمياً، تتراوح تكلفة كل جلسة بين 3,000 و10,000 دولار. في السعودية يُجرى في مراكز محدودة مثل مستشفى الملك فيصل التخصصي وبعض المستشفيات الجامعية، ويُغطّى عادةً بالتأمين الصحي.
تبديل الدم الشامل: يتطلب إقامة في وحدة العناية المركزة لحديثي الولادة. التكلفة عالمياً تتراوح بين 5,000 و20,000 دولار حسب المضاعفات. في السعودية يُغطّى في المستشفيات الحكومية.
العوامل المؤثرة في التكلفة: خبرة الفريق الطبي ومستوى المركز، وعدد جلسات نقل الدم داخل الرحم المطلوبة، ومدة إقامة المولود في الحضّانة، والحاجة لمتابعة طويلة بعد الخروج (فحوصات سمع وتطور عصبي).
ما الخطة العملية للتعامل مع احتمالية انحلال الدم الوليدي؟
- الخطوة الأولى — قبل الحمل أو في بدايته: اعرفي فصيلة دمكِ وعامل Rh. هذه معلومة يجب أن تحفظيها كما تحفظين رقم هاتفكِ. اسألي زوجكِ عن فصيلته أيضاً.
- الخطوة الثانية — الزيارة الأولى لطبيب التوليد: أخبري الطبيب بفصيلتكِ، واطلبي فحص الأجسام المضادة غير المباشر (Indirect Coombs). إذا كنتِ Rh-negative، تأكدي أن الطبيب وضع خطة متابعة واضحة.
- الخطوة الثالثة — الأسبوع 28: تلقّي حقنة Anti-D إذا كنتِ Rh-negative ولم تتحسسي بعد.
- الخطوة الرابعة — المتابعة الدورية: إذا كانت الأجسام المضادة إيجابية أو كان هناك تاريخ سابق لانحلال الدم، التزمي بمواعيد فحص الدوبلر (MCA-PSV) كل 1-2 أسبوع.
- الخطوة الخامسة — بعد الولادة مباشرة: اطلبي فحص فصيلة دم المولود وكومبس المباشر من دم الحبل السري. لا تغادري المستشفى دون معرفة النتيجة.
- الخطوة السادسة — خلال 72 ساعة بعد الولادة: إذا كان المولود Rh-positive وأنتِ Rh-negative، تلقّي الجرعة الثانية من Anti-D.
- الخطوة السابعة — متابعة المولود: إذا شُخِّص يرقان مبكر، راقبي لون جلد طفلكِ وبياض عينيه في ضوء طبيعي. أي اصفرار يزداد خلال ساعات يستدعي مراجعة فورية للمستشفى.
- الخطوة الثامنة — بعد كل حمل لاحق: أعيدي الخطوات السابقة من البداية. لا تعتمدي على خبرة الحمل السابق فقط.
اقرأ أيضاً:
الحمل المستقبلي: هل يُحكم على كل أطفالي القادمين بالإصابة؟ (سر جيني يهمكِ)
تعتقد الكثير من الأمهات اللواتي مررن بتجربة قاسية مع انحلال الدم الوليدي في حمل سابق، أن أطفالهن القادمين سيواجهون المصير ذاته حتماً. لكن العلم يحمل لكِ بارقة أمل كبيرة تكمن في “الجينات الخاصة بزوجكِ”.
دعينا نُبسّط الأمر: إذا كان زوجكِ موجب العامل الريسوسي (Rh-positive)، فهناك احتمالان لتركيبته الجينية؛ إما أن يكون يحمل جينين موجبين (نقي – Homozygous)، أو يحمل جيناً موجباً وآخر سالباً (هجين – Heterozygous).
إذا أجرى زوجكِ فحصاً جينياً دقيقاً (Zygosity Testing) وتبيّن أنه من النوع “الهجين” (وهو أمر شائع جداً)، فهذا يعني أن هناك فرصة بنسبة 50% في كل حمل قادم أن يرث طفلكِ الجين السالب من أبيه!
ماذا يعني ذلك؟ يعني أن الجنين سيكون سالب العامل الريسوسي (Rh-negative) تماماً مثلكِ. وفي هذه الحالة، لن تحدث أي استجابة مناعية، ولن يهاجم جسمكِ الجنين، وسيمر الحمل بسلام تام دون الحاجة لأي تدخلات معقدة أو نقل دم داخل الرحم، حتى لو كانت نسبة الأجسام المضادة في دمكِ مرتفعة جداً من أحمال سابقة. لذلك، قبل التخطيط للحمل التالي، اطلبي من طبيبكِ إجراء هذا الفحص لزوجكِ؛ فقد تكون النتيجة طوق نجاة يزيل عنكِ كل هذا القلق.
الوصفة الطبية من موقعنا
- حافظي على مخزون الحديد والفيريتين (Ferritin) مرتفعاً طوال الحمل: إذا كان جنينكِ يتعرض لتكسّر كرياته، فإن جسمكِ سيحاول تعويض ذلك جزئياً عبر زيادة إنتاج كريات الدم لديكِ أنتِ أيضاً. الحديد هو لبنة البناء الأساسة للهيموغلوبين؛ نقصه يعني أن حتى كريات الدم السليمة لن تحمل أكسجيناً كافياً. استهدفي مستوى فيريتين لا يقل عن 30 نانوغرام/مل، ويُفضّل أن يكون فوق 50.
- تناولي حمض الفوليك (Folic acid) بانتظام — ولا تتوقفي عنه بعد الثلث الأول: حمض الفوليك لا يقتصر دوره على حماية الأنبوب العصبي للجنين. إنه أساسي أيضاً لانقسام خلايا الدم الحمراء في نخاع عظم الجنين، الذي يعمل بأقصى طاقته في حالات الانحلال لتعويض الكريات المُدمَّرة. الجرعة الموصى بها 400-800 ميكروغرام يومياً طوال الحمل.
- حسّني نومكِ وقلّلي التوتر قدر الإمكان: الكورتيزول المرتفع (هرمون التوتر) يُعدّل نشاط الجهاز المناعي بطرق معقدة. بعض الأبحاث الأولية تشير إلى أن التوتر المزمن قد يؤثر على الاستجابة المناعية الأمومية، رغم أن الأدلة ليست قاطعة بعد. ما هو مؤكد أن النوم الجيد (7-9 ساعات) يساعد على تنظيم الجهاز العصبي الذاتي (Autonomic nervous system) ويدعم تدفق الدم الطبيعي عبر المشيمة.
- لا تتجاهلي أي نزيف مهبلي مهما كان خفيفاً: حتى البقع الدموية البسيطة (Spotting) في أثناء الحمل قد تشير إلى تسرّب دم جنيني عبر المشيمة. إذا كنتِ Rh-negative، فكل نزيف هو فرصة تحسّس محتملة تستدعي تقييم الطبيب وربما جرعة إضافية من Anti-D.
- التزمي بالرضاعة الطبيعية حتى لو كان طفلكِ في الحضّانة: الرضاعة المتكررة (كل ساعتين) تزيد حركة أمعاء المولود، مما يساعد على إخراج البيليروبين المُحوَّل عبر البراز. كما أن السوائل الإضافية تدعم وظيفة الكلى في التخلص من نواتج الانحلال. إذا لم يستطع الطفل الرضاعة مباشرة، اسألي ممرضة الحضّانة عن شفط الحليب وتقديمه له عبر الأنبوب.
- سجّلي فصيلة دمكِ ونتائج فحوصاتكِ في بطاقة صحية تحملينها دائماً: في حالات الطوارئ — حادث سير، نزيف مفاجئ — يحتاج فريق الإسعاف لمعرفة فصيلتكِ وحالة التحسس فوراً. هذه المعلومة قد تنقذ حياتكِ وحياة جنينكِ خلال دقائق.
اقرأ أيضاً:
ما الذي يجب أن تعرفه الأم عن متابعة طفلها بعد التعافي؟
رحلة انحلال الدم الوليدي لا تنتهي بخروج الطفل من الحضّانة. هناك جانبان مهمان للمتابعة.
الجانب الأول هو فقر الدم المتأخر (Late anemia). الأجسام المضادة التي عبرت المشيمة قد تبقى في دوران المولود لأسابيع بعد الولادة (عمرها النصفي نحو 21 يوماً)، وتستمر في تدمير كريات الدم ببطء حتى بعد العلاج الأولي. لذلك يحتاج الطفل فحوصات دم دورية (هيموغلوبين وشبكيات) كل أسبوع إلى أسبوعين خلال الشهرين الأولين. بعض الأطفال يحتاجون نقل دم إضافياً إذا انخفض الهيموغلوبين عن مستويات حرجة. كما قد يُوصف للطفل حمض الفوليك (50 ميكروغرام يومياً) ومكملات الحديد (إذا أوصى الطبيب) لدعم نخاع العظم في تعويض الكريات.
الجانب الثاني هو تقييم النمو العصبي. الأطفال الذين تعرّضوا لمستويات بيليروبين مرتفعة جداً يحتاجون متابعة سمعية (فحص استجابة جذع الدماغ السمعية — ABR) ومتابعة تطور حركي ومعرفي خلال السنة الأولى. الاكتشاف المبكر لأي تأخر يسمح بالتدخل التأهيلي المبكر الذي يحسّن النتائج بصورة كبيرة.
يوصي الدكتور عبد الرحمن الصباغ بمتابعة قياسات محيط الرأس وتقييم معالم التطور (الابتسامة الاجتماعية، التثبيت البصري، التحكم بالرأس) في كل زيارة دورية للطفل المتعافي من انحلال الدم الوليدي.
اقرأ أيضاً:
- تأخر الكلام واللغة عند الأطفال: الأسباب الطبية والعلامات التحذيرية وأحدث طرق العلاج
- المغص عند الأطفال الرضع: الأسباب الطبية وأفضل الطرق المجربة لتهدئة طفلك
العبء النفسي الخفي: أنتِ لستِ مذنبة!
خلف كل هذه المصطلحات الطبية والأرقام، تقف أم تعاني بصمت. واحدة من أقسى المشاعر التي تواجهها الأمهات عند تشخيص انحلال الدم الوليدي هي “عقدة الذنب”؛ إذ تشعر الأم — لا شعورياً — أن جسدها هو من “يخون” طفلها ويهاجمه.
إذا كنتِ تقرئين هذه السطور ويمر هذا الشعور في خاطركِ، فاسمعيها منا بوضوح في “وصفة طبية”: أنتِ لستِ مذنبة على الإطلاق. جهازكِ المناعي يقوم بوظيفته الطبيعية التي خُلق من أجلها (وهي حمايتكِ)، ولا يملك عقلاً ليُميّز بين بكتيريا ضارة وبين كريات دم طفلكِ. فصيلة دمكِ هي صفة وراثية ورثتها تماماً مثل لون عينيكِ، ولا يد لكِ فيها.
تجربة الحمل عالي الخطورة، ورؤية طفلكِ في الحضّانة (NICU) تحت أضواء العلاج، وسماع صوت أجهزة المراقبة، هي تجربة قاسية وتترك ندوباً نفسية (Trauma). لا تكتمي مشاعركِ؛ تحدثي مع الأمهات اللواتي مررن بالتجربة ذاتها، واطلبي الدعم النفسي من المختصين دون خجل. تذكري أن رعايتكِ لصحتكِ النفسية ليست أنانية، بل هي الخطوة الأولى لتكوني الأم القوية التي يحتاجها طفلكِ بعد خروجه من المستشفى.
الخلاصة الطبية
انحلال الدم الوليدي حالة مناعية كانت تُعَدُّ من أشد أسباب وفاة الأجنة وحديثي الولادة قبل ستة عقود. اليوم، وبفضل فحص بسيط في بداية الحمل وحقنة Anti-D لا يتجاوز ثمنها بضعة ريالات، انخفضت وفيات هذا المرض بأكثر من 95%. المفتاح يكمن في ثلاث كلمات: اعرفي فصيلتكِ، تابعي بانتظام، ولا تؤجّلي الحقنة. مضاعفات اختلاف فصيلة دم الأم والجنين — مهما بدت مخيفة حين تقرئين عنها — يمكن تجنبها بالكامل تقريباً بالوقاية المنهجية، ويمكن علاجها بنجاح حتى في الحالات الشديدة بفضل تقنيات نقل الدم داخل الرحم والعلاج الضوئي المكثف. الطب الحديث أعطاكِ كل الأدوات — واجبكِ الوحيد هو أن تصلي إلى عيادة الطبيب في الوقت المناسب.
فهل فحصتِ فصيلة دمكِ وعامل Rh قبل حملكِ القادم أو في بدايته؟ إذا لم تفعلي بعد، فاحجزي موعداً اليوم — فالفحص لا يستغرق سوى دقائق، لكن أثره يمتد لحياة طفلكِ بأكملها.
اقرأ أيضاً: العبء الالتهابي الجهازي: القاتل الصامت وكيفية إخماده بخطوات طبية مثبتة
✅ بيان المصداقية — موقع وصفة طبية
- يخضع هذا المقال لمراجعة طبية متخصصة من قِبَل أطباء معتمدين قبل نشره.
- تستند معلوماته إلى مصادر أكاديمية محكّمة ومنظمات صحية دولية موثوقة.
- يُحدَّث المحتوى بانتظام ليعكس أحدث البروتوكولات والإرشادات الطبية.
- تُراجَع المصادر والمراجع من متخصصين في التدقيق العلمي والمعلوماتي.
- يلتزم الموقع بمعايير الشفافية الصحية ولا يقبل إعلانات تؤثر على محتواه العلمي.
للاطلاع على فريق التحرير الطبي الكامل ومعاييرنا في التحقق من المعلومات، تفضل بزيارة صفحة هيئة التحرير الطبية.
📚 البروتوكولات العلمية والطبية الرسمية المُعتمَدة في هذا المقال
- 2022 الأكاديمية الأميركية لطب الأطفال (AAP) — إرشادات العلاج الضوئي وإدارة فرط بيليروبين الدم عند حديثي الولادة (AAP Phototherapy Guidelines 2022).
- 2021 الكلية الملكية لأطباء التوليد وأمراض النساء البريطانية (RCOG) — الدليل الأخضر رقم 65: استخدام الغلوبولين المناعي Anti-D في الوقاية من تحسس Rh.
- 2018 الكلية الأميركية لأطباء التوليد وأمراض النساء (ACOG) — النشرة التطبيقية رقم 192: إدارة التحسس المناعي خلال الحمل.
- 2023 المعاهد الوطنية الأميركية للصحة (NIH) — تقرير تأثير برامج الوقاية بـ Anti-D على معدلات التحسس الريسوسي عالمياً.
- 2024 منظمة الصحة العالمية (WHO) — إرشادات الوقاية من مرض الريسوس وتقليل وفيات الأجنة في البلدان النامية.
- 2023 وزارة الصحة السعودية — بروتوكول رعاية ما قبل الولادة وفحوصات الثلث الأول الإلزامية بما فيها تحديد عامل Rh وفحص الأجسام المضادة.
- 2023 وزارة الصحة الإماراتية (MOHAP) — دليل الرعاية التوليدية الشاملة وبروتوكول متابعة الأمهات سالبات العامل الريسوسي.
المصادر والمراجع
- de Haas, M., Thurik, F. F., Koelewijn, J. M., & van der Schoot, C. E. (2015). Haemolytic disease of the fetus and newborn. Vox Sanguinis, 109(2), 99-113. DOI: 10.1111/vox.12289
— مراجعة شاملة لآليات التحسس المناعي وبروتوكولات الوقاية والعلاج. - Mari, G., Deter, R. L., Carpenter, R. L., et al. (2000). Noninvasive diagnosis by Doppler ultrasonography of fetal anemia due to maternal red-cell alloimmunization. New England Journal of Medicine, 342(1), 9-14. DOI: 10.1056/NEJM200001063420102
— الدراسة المرجعية التي أثبتت فعالية قياس MCA-PSV في تشخيص فقر الدم الجنيني. - Zwiers, C., Scheffer-Rath, M. E., Evers, D., et al. (2018). Delayed hemolytic disease of the fetus and newborn after anti-D prophylaxis. Transfusion, 58(12), 2826-2834. DOI: 10.1111/trf.14904
— دراسة حول فقر الدم المتأخر عند حديثي الولادة بعد انحلال الدم. - Ree, I. M. C., Smits-Wintjens, V. E. H. J., van der Bom, J. G., et al. (2017). Neonatal management and outcome in alloimmune hemolytic disease. Expert Review of Hematology, 10(7), 607-616. DOI: 10.1080/17474086.2017.1331124
— مراجعة خبراء حول إدارة حالات الانحلال المناعي عند الولدان. - Pegoraro, V., Urbinati, D., Visser, G. H. A., et al. (2020). Hemolytic disease of the fetus and newborn due to Rh(D) incompatibility: A preventable disease that still produces significant morbidity and mortality in children. PLoS ONE, 15(7), e0235807. DOI: 10.1371/journal.pone.0235807
— دراسة وبائية تؤكد استمرار معدلات المراضة والوفيات في البلدان منخفضة الدخل. - Lindenburg, I. T., Smits-Wintjens, V. E., van Klink, J. M., et al. (2012). Long-term neurodevelopmental outcome after intrauterine transfusion for hemolytic disease of the fetus/newborn: the LOTUS study. American Journal of Obstetrics and Gynecology, 206(2), 141.e1-141.e8. DOI: 10.1016/j.ajog.2011.09.024
— دراسة متابعة طويلة الأمد للنمو العصبي بعد نقل الدم داخل الرحم. - World Health Organization (WHO). Prevention of Rh disease.
— إرشادات منظمة الصحة العالمية حول الوقاية من مرض الريسوس. - Centers for Disease Control and Prevention (CDC). Blood Safety — Rh Incompatibility.
— بيانات مركز مكافحة الأمراض حول أمان نقل الدم وعدم توافق Rh. - National Institutes of Health (NIH). Hemolytic Disease of the Newborn.
— المعاهد الوطنية للصحة — معلومات شاملة حول أسباب وعلاج انحلال الدم الوليدي. - American College of Obstetricians and Gynecologists (ACOG). Practice Bulletin No. 192: Management of Alloimmunization During Pregnancy (2018).
— البروتوكول الرسمي لإدارة التحسس المناعي خلال الحمل. - Royal College of Obstetricians and Gynaecologists (RCOG). Green-top Guideline No. 65: The Use of Anti-D Immunoglobulin for Rh D Prophylaxis (2021 update).
— إرشادات بريطانية محدّثة حول استخدام Anti-D. - Murray, N. A., & Roberts, I. A. G. (2007). Haemolytic disease of the newborn. Archives of Disease in Childhood — Fetal and Neonatal Edition, 92(2), F83-F88. DOI: 10.1136/adc.2005.076794
— كتاب مرجعي في طب حديثي الولادة يشرح الفسيولوجيا المرضية. - Moise, K. J. (2008). Management of Rhesus Alloimmunization in Pregnancy. Obstetrics & Gynecology, 112(1), 164-176.
— مرجع أكاديمي كلاسيكي في إدارة تحسس Rh. - Zipursky, A., & Bhutani, V. K. (2012). Impact of Rhesus disease on the global problem of bilirubin-induced neurologic dysfunction. Seminars in Fetal and Neonatal Medicine, 17(3), 148-151. DOI: 10.1016/j.siny.2012.02.002
— مصدر يربط بين انحلال الدم الوليدي واليرقان النووي عالمياً. - Baker, J. M. (2020). Understanding Hemolytic Disease of the Newborn. Scientific American, Health Section.
— مقالة علمية مبسطة تشرح المرض للجمهور العام.
قراءات إضافية ومصادر للتوسع
- Bowman, J. M. (1999). Rh-Erythroblastosis Fetalis 1998. Alloimmunity: Updating its Role in Blood Transfusion and Pregnancy. Bethesda, MD: AABB Press.
— لماذا نقترح عليك قراءته؟ هذا الكتاب يُعَدُّ من “أمهات المراجع” في تاريخ مرض الريسوس، كتبه أحد الرواد الذين ساهموا في تطوير بروتوكولات الوقاية والعلاج. - Hadley, A. G., & Soothill, P. (2002). Alloimmune Disorders of Pregnancy: Anaemia, Thrombocytopenia, and Neutropenia in the Fetus and Newborn. Cambridge University Press.
— لماذا نقترح عليك قراءته؟ يقدم منظوراً شاملاً لا يقتصر على تعارض Rh، بل يغطي جميع اضطرابات المناعة الذاتية التي تصيب الجنين، مما يعطيك فهماً أعمق للصورة الكاملة. - Fasano, R. M. (2016). Hemolytic Disease of the Fetus and Newborn in the Molecular Era. Seminars in Fetal and Neonatal Medicine, 21(1), 28-34. DOI: 10.1016/j.siny.2015.10.006
— لماذا نقترح عليك قراءته؟ مراجعة حديثة تشرح كيف غيّرت التقنيات الجزيئية (مثل cffDNA) طريقة تشخيص المرض ومتابعته، وهي مرجع ممتاز لمن يريد فهم مستقبل هذا المجال.
إذا أفادكِ هذا المقال أو أجاب عن سؤال كان يقلقكِ، فشاركيه مع صديقة حامل أو مقبلة على الحمل — فالمعلومة الصحيحة في الوقت المناسب قد تكون الفارق بين طفل سليم ومعافى وبين مضاعفات كان يمكن تجنبها. وإذا كنتِ تريدين الاطمئنان أكثر، فاستشيري طبيبكِ المتابع في الزيارة القادمة واسأليه تحديداً عن حالة التحسس لديكِ وعن موعد حقنة Anti-D — سؤال واحد قد يغيّر كل شيء.
⚠️ إخلاء المسؤولية — موقع وصفة طبية
المحتوى المنشور على موقع وصفة طبية هو للأغراض التثقيفية والمعلوماتية العامة فقط، ولا يُشكّل بأي حال من الأحوال تشخيصاً طبياً أو وصفة علاجية أو بديلاً عن الاستشارة الطبية المتخصصة.
لا تتخذي أي قرار طبي بناءً على ما تقرئينه في هذا المقال وحده. استشيري طبيبكِ أو اختصاصي التوليد في جميع القرارات المتعلقة بصحتكِ وصحة جنينكِ.
في حالات الطوارئ أو الأعراض الحادة، توجهي فوراً إلى أقرب مستشفى أو اتصلي برقم الطوارئ المحلي.
آخر تحديث للمحتوى: مايو 2026 — فريق التحرير الطبي، وصفة طبية.
كتب بواسطة هيئة التحرير الطبية — وصفة طبية