اليرقان النووي (Kernicterus): عندما يتحول صفار حديثي الولادة إلى خطر يهدد الدماغ
كيف تميّز بين الاصفرار العابر والتلف الدماغي الذي لا يمكن عكسه؟

اليرقان النووي هو شكل حاد من تلف الدماغ يصيب حديثي الولادة نتيجة ارتفاع مستويات البيليروبين غير المقترن في الدم إلى حدود سُمّية تخترق النسيج الدماغي. يستهدف هذا التلف بصورة انتقائية نوى قاعدة الدماغ (Basal Ganglia) وجذع الدماغ (Brainstem). تشير تقديرات منظمة الصحة العالمية إلى أن نحو 114,000 وفاة سنوية عالمياً ترتبط بيرقان الولادة الشديد. الوقاية ممكنة تماماً بالكشف المبكر، لكن التلف بعد حدوثه لا يمكن إصلاحه.
أبرز ما ستتعلمه في هذا المقال
خلاصة علمية في أقل من دقيقة — قبل أن تبدأ القراءة التفصيلية
- اليرقان النووي ليس مجرد “صفار مبالغ فيه” — بل هو تلف دماغي دائم يصيب النوى القاعدية ويتسبب في شلل دماغي وصمم وإعاقة مزمنة.
- البيليروبين غير المقترن فقط هو الذي يخترق حاجز الدم-الدماغ ويسبب التلف. البيليروبين المقترن لا يُشكّل هذا الخطر.
- نقص إنزيم G6PD هو عامل الخطر الأول لليرقان النووي في منطقتنا العربية، ويصيب ذكور المنطقة بنسبة تصل إلى 7%.
- اصفرار يظهر خلال أول 24 ساعة من الولادة — علامة خطر بلا استثناء.
- اصفرار وصل إلى راحتَي اليدين أو باطن القدمين — توجّه للطوارئ فوراً.
- بكاء حاد غير عادي + رفض الرضاعة + تقوّس الظهر للخلف = إنذار حمراء — لا تنتظر لحظة.
- اطلبي فحص البيليروبين لطفلك قبل مغادرة المستشفى — هذا حقك وهو إجراء قياسي.
- لا تُلغي أو تؤجّلي موعد المراجعة الطبية خلال 48 ساعة من الخروج — حتى لو بدا طفلك بخير تماماً.
- أرضعي 8 إلى 12 مرة يومياً — الرضاعة الكافية هي أقوى سلاح وقائي طبيعي ضد تراكم البيليروبين.
وقت القراءة الكاملة: ~18 دقيقة | 6,000 كلمة
هل أخبرك أحدهم يوماً أن “الصفار عند المواليد أمر طبيعي ويروح لحاله”؟ ربما كان محقاً في أغلب الحالات، لكن ماذا لو لم يكن طفلك ضمن تلك الأغلبية؟ ماذا لو كان ذلك الاصفرار اللطيف يُخفي خلفه عاصفة كيميائية تزحف ببطء نحو خلايا دماغه؟ ما ستقرأه في هذا المقال سيمنحك أدوات عملية واضحة لتفرّق بين يرقان يزول وحده ويرقان يستدعي ركضك إلى الطوارئ. لن أخوّفك، لكنني سأعطيك المعرفة التي تحميك من أن تُفاجأ.
تخيّلي هذا الموقف: أم شابة تُدعى سارة، ولدت طفلها الأول في أحد مستشفيات الرياض. في اليوم الثاني بعد الولادة لاحظت اصفراراً خفيفاً في وجه رضيعها. أخبرتها حماتها أن هذا “صفار طبيعي يصيب كل الأطفال”. بعد الخروج من المستشفى، لم تراجع الطبيب في الموعد المحدد بعد 48 ساعة. في اليوم الخامس، لاحظت سارة أن الاصفرار انتشر إلى بطن الطفل وراحتَيه، وبدأ يرفض الرضاعة ويبكي بصوت حاد غريب. عندما وصلت للطوارئ، كان مستوى البيليروبين قد تجاوز 30 ملغ/ديسيلتر. أجرى الأطباء نقل دم طارئاً، لكن التصوير بالرنين لاحقاً أظهر بدايات تلف في نوى الدماغ. هذا السيناريو ليس نادراً كما تظنين. والدرس الوحيد منه: لا تؤجّلي موعد المراجعة الطبية أبداً، ولا تعتمدي على “خبرة الأهل” وحدها.
في كبسولة: ما يجب أن تعرفه فوراً عن اليرقان النووي
إذا كنت تقرأ هذا المقال وأنت في عجلة من أمرك، فإليك الزبدة الطبية التي يجب أن تتصرف بناءً عليها. اليرقان النووي ليس مرضاً حتمياً، بل هو نتيجة لإهمال اصفرار شديد كان يمكن علاجه بسهولة. القاعدة الذهبية هي عدم تجاهل أي اصفرار يمتد إلى بطن الطفل أو ساقيه، وعدم التهاون في موعد المراجعة الطبية خلال أول ثمانٍ وأربعين ساعة من الخروج من المستشفى. الرضاعة المتكررة هي سلاحك الأول، وفحص الدم هو حَكَمك الفيصل، والعلاج بالضوء في المستشفى هو طوق النجاة الآمن. تذكّر دائماً: خفض البيليروبين مبكراً ينقذ الدماغ، والتأخير لساعات قد يترك أثراً لا يُمحى.
اقرأ أيضاً:
- اليرقان الوليدي (صفار المواليد): الأسباب، درجات الخطورة، وخطوات العلاج الطبية
- انحلال الدم الوليدي: الأسباب، الأعراض، وخطوات العلاج والوقاية
ما هو اليرقان النووي وكيف يتحول البيليروبين إلى سُمّ عصبي؟
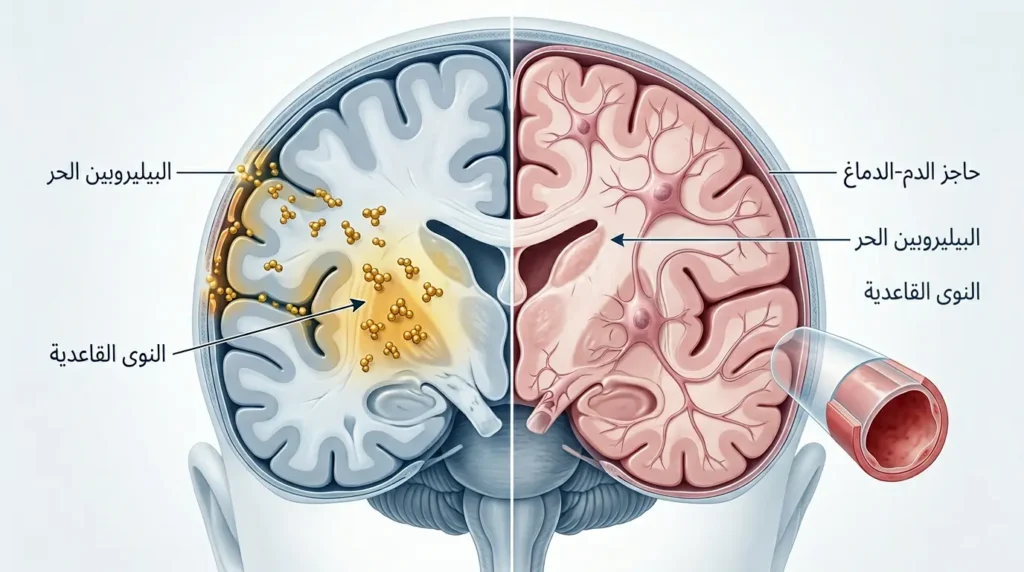
لكي تفهم اليرقان النووي فعلاً، عليك أولاً أن تتعرف على الشخصية المحورية في هذه القصة: مادة اسمها البيليروبين (Bilirubin). هذه المادة الصفراء تنتج طبيعياً في جسم كل إنسان عندما تتكسر خلايا الدم الحمراء القديمة. في الوضع الطبيعي، يأخذ الكبد هذا البيليروبين ويحوّله إلى شكل قابل للذوبان في الماء — يُسمى البيليروبين المقترن (Conjugated Bilirubin) — ثم يُطرح عبر الصفراء إلى الأمعاء ويخرج مع البراز. فكّر في الكبد كأنه محطة معالجة مياه الصرف في مدينتك: يستقبل المواد السامة ويحولها إلى مواد آمنة قابلة للتخلص منها.
عند حديثي الولادة، تكون محطة المعالجة هذه — أي الكبد — غير مكتملة النضج بعد. الإنزيم المسؤول عن تحويل البيليروبين، واسمه يوريدين ثنائي فوسفات غلوكورونيل ترانسفيراز (UDP-Glucuronosyltransferase أو UGT1A1)، يعمل بكفاءة منخفضة في الأيام الأولى من الحياة. في الوقت نفسه، يملك الرضيع عدداً أكبر من خلايا الدم الحمراء مقارنةً بالبالغين، وعمر هذه الخلايا أقصر (نحو 70-90 يوماً مقابل 120 يوماً عند البالغ)، مما يعني تكسراً أسرع وإنتاجاً أعلى للبيليروبين. النتيجة؟ بيليروبين كثير يتراكم، وكبد صغير لا يستطيع مجاراته.
في معظم المواليد، يتراكم البيليروبين بشكل معتدل ثم ينخفض تلقائياً خلال أسبوع أو أسبوعين. هذا هو اليرقان الفسيولوجي (Physiological Jaundice) — الصفار “الطبيعي” الذي سمعت عنه. لكن في حالات معينة، يرتفع البيليروبين غير المقترن إلى مستويات خطيرة تتجاوز قدرة بروتين الألبومين (Albumin) في الدم على حمله بأمان. عندما يفوق البيليروبين الحر سعة الارتباط بالألبومين، يبدأ بالتسلل عبر الحاجز الدموي الدماغي (Blood-Brain Barrier أو BBB). هذا الحاجز عند الرضع — خصوصاً الخدج — يكون أقل نضجاً وأكثر نفاذية، مما يسمح لهذا السم الأصفر بالدخول إلى أنسجة الدماغ مباشرة.
حين يصل البيليروبين الحر إلى الدماغ، فإنه يستهدف مناطق بعينها: النوى القاعدية (Basal Ganglia)، والحصين (Hippocampus)، ونوى الأعصاب القحفية في جذع الدماغ، ونوى المخيخ (Cerebellum). يرتبط بأغشية الخلايا العصبية والميتوكوندريا (مصانع الطاقة في الخلية) ويعطّل سلسلة نقل الإلكترونات (Electron Transport Chain)، مما يقتل الخلايا العصبية أو يشلّ وظيفتها. هذا التلف — إذا استمر — هو ما نسميه اليرقان النووي أو Kernicterus. كلمة “نووي” هنا لا تعني إشعاعاً، بل تُشير إلى “النوى” الدماغية التي تتلطخ بالصبغة الصفراء عند فحص الدماغ بعد الوفاة — وهو المشهد الذي وصفه لأول مرة طبيب التشريح الألماني كريستيان شمورل (Christian Schmorl) عام 1903.
حقيقة طبية: البيليروبين غير المقترن هو الشكل الوحيد الذي يعبر حاجز الدم في الدماغ ويسبب تلفاً عصبياً. البيليروبين المقترن (المباشر) لا يخترق هذا الحاجز، ولذلك فإن ارتفاعه وحده لا يسبب اليرقان النووي.
لماذا يُخطئ كثير من الأهل في التفريق بين اليرقان العادي واليرقان النووي؟
هنا يكمن اللبس الأخطر. الفرق بين اليرقان العادي واليرقان النووي ليس فرقاً في النوع بقدر ما هو فرق في الدرجة والتوقيت والسرعة. تخيّل الأمر كحريق: كل حريق يبدأ بشرارة، لكن ليس كل شرارة تصبح حريقاً مدمراً. المشكلة أن الشرارة والحريق يبدوان متشابهين في اللحظات الأولى. اليرقان الفسيولوجي يظهر عادةً بعد 24-72 ساعة من الولادة، ويبدأ في الوجه ثم ينزل تدريجياً نحو الصدر. يبلغ ذروته بين اليوم الثالث والخامس عند الرضّع مكتملي الحمل، ثم يتراجع تلقائياً خلال أسبوع إلى أسبوعين. مستويات البيليروبين فيه لا تتجاوز عادةً 12-15 ملغ/ديسيلتر، والطفل يرضع جيداً، ينام وينتبه بشكل طبيعي، ولا تظهر عليه علامات عصبية.
على النقيض من ذلك، اليرقان المرضي — الذي قد يتطور إلى يرقان نووي — يتميز بعلامات مختلفة تماماً. قد يظهر خلال أول 24 ساعة من الولادة (وهذه وحدها علامة خطر كبيرة). ينتشر الاصفرار بسرعة إلى ما دون السرة، ويصل إلى الأطراف وراحتَي اليدين وباطن القدمين. مستويات البيليروبين ترتفع بسرعة تزيد عن 5 ملغ/ديسيلتر في اليوم، وقد تتخطى 20-25 ملغ/ديسيلتر أو أكثر. الطفل يبدو خاملاً أو مُهيَّجاً، يرفض الرضاعة، أو يبكي بصوت حاد غير معتاد.
المعضلة الحقيقية هي أن اللون الأصفر وحده لا يكفي للتمييز. بشرة الطفل الداكنة قد تُخفي شدة الاصفرار. الإضاءة الصناعية في المنزل قد تُضلّل عين الأم. ولهذا السبب تحديداً تُصرّ جميع الجمعيات الطبية على قياس مستوى البيليروبين مخبرياً قبل خروج أي مولود من المستشفى، ومتابعته خلال 24-48 ساعة بعد الخروج.
| وجه المقارنة | اليرقان الفسيولوجي | اليرقان المرضي |
|---|---|---|
| وقت الظهور | بعد 24 إلى 72 ساعة من الولادة | خلال أول 24 ساعة من الولادة (علامة خطر) |
| مناطق الاصفرار | الوجه والصدر فقط | ينتشر إلى البطن والأطراف وراحتَي اليدين وباطن القدمين |
| سرعة الارتفاع | تدريجية وبطيئة | أكثر من 5 ملغ/ديسيلتر في اليوم الواحد |
| مستوى البيليروبين | عادةً أقل من 12 إلى 15 ملغ/ديسيلتر | قد يتجاوز 20 إلى 25 ملغ/ديسيلتر أو أكثر |
| سلوك الطفل | يرضع جيداً، نشيط، نوم طبيعي | خامل، يرفض الرضاعة، بكاء حاد أو صراخ غير عادي |
| توقيت الذروة | اليوم 3 إلى 5 عند الرضع المكتملين | لا توجد ذروة واضحة، الارتفاع مستمر |
| مسار التحسن | يتراجع تلقائياً خلال 1 إلى 2 أسبوع | لا يتراجع بدون علاج طبي |
| الحاجة للعلاج | مراقبة فقط في الغالب | علاج ضوئي فوري أو نقل دم طارئ |
| خطر تلف الدماغ | لا يوجد عند المستويات الطبيعية | خطر حقيقي ومباشر إذا لم يُعالج فوراً |
نقطة تستحق الانتباه: في المملكة العربية السعودية، أصدرت الهيئة السعودية للتخصصات الصحية توصيات محدّثة تُلزم مستشفيات الولادة بإجراء فحص البيليروبين عبر الجلد (Transcutaneous Bilirubinometry أو TcB) أو فحص الدم قبل الخروج، ومتابعة المولود خلال 48 ساعة. إن لم يحصل طفلك على هذا الفحص، فاطلبيه صراحةً.
اقرأ أيضاً: الفحوصات الطبية الدورية: متى يجب أن تبدأ وما الذي تحتاجه في كل عمر؟
فخ الرضاعة: هل حليب الأم هو المتهم الخفي في زيادة الاصفرار؟
يخلط الكثيرون بين نوعين من اليرقان المرتبطين بالرضاعة الطبيعية، وهذا الخلط قد يؤدي إلى قرارات متسرعة ومؤذية، مثل إيقاف الرضاعة الطبيعية فجأة دون استشارة طبية. النوع الأول يُعرف بـ “يرقان الرضاعة الطبيعية” (Breastfeeding Jaundice)، وهو لا يحدث بسبب الحليب نفسه، بل بسبب قلة كمية الحليب التي يحصل عليها الطفل في أيامه الأولى. قلة الحليب تعني جفافاً طفيفاً وبطئاً في حركة الأمعاء، مما يعيق خروج البيليروبين مع البراز ويؤدي إلى إعادة امتصاصه إلى الدم. حل هذا النوع ليس إيقاف الرضاعة، بل تكثيفها ومساعدة الطفل على الالتقام الصحيح.
أما النوع الثاني فهو “يرقان حليب الأم” (Breast Milk Jaundice)، وهو حالة مختلفة تماماً تظهر عادة بعد الأسبوع الأول. في هذه الحالة، يحتوي حليب الأم نفسه على مواد وبروتينات معينة تُثبط عمل إنزيمات الكبد المسؤولة عن تكسير البيليروبين. ورغم أن هذا النوع قد يستمر لأسابيع وربما أشهر، إلا أنه نادراً جداً ما يصل إلى مستويات خطيرة تسبب اليرقان النووي إذا كان الطفل ينمو ويرضع بشكل ممتاز. الأطباء لا ينصحون أبداً بإيقاف الرضاعة الطبيعية في هذه الحالة إلا في سيناريوهات نادرة جداً ولأيام معدودة فقط لغرض التشخيص، وبإشراف طبي دقيق.
ما هي الأسباب التي تقود إلى هذا المستوى الخطير من البيليروبين؟
اليرقان النووي لا ينشأ من فراغ. هو نتيجة نهائية لسلسلة من الأحداث تبدأ بارتفاع شديد وغير معالج في البيليروبين. لفهم كيف نصل إلى هذه المرحلة الكارثية، علينا تتبع المسارات التي تُنتج فائضاً كبيراً من البيليروبين أو تعيق التخلص منه.
السبب الأول والأكثر شيوعاً هو عدم التوافق في فصائل الدم بين الأم والجنين. إذا كانت الأم من فصيلة O والطفل من فصيلة A أو B — وهو ما يُعرف بعدم توافق ABO (ABO Incompatibility) — فإن أجساماً مضادة من دم الأم تعبر المشيمة وتهاجم خلايا دم الطفل الحمراء وتدمرها بسرعة، مما يُنتج كميات هائلة من البيليروبين. الحالة الأشد خطورة هي عدم توافق عامل ريزوس (Rh Incompatibility)، وتحدث حين تكون الأم سالبة العامل (Rh-negative) والطفل موجباً (Rh-positive). بدون الوقاية بحقنة الغلوبيولين المناعي المضاد لـ D (Anti-D Immunoglobulin) في أثناء الحمل وبعد الولادة، يمكن أن يكون تكسر الدم عنيفاً جداً.
السبب الثاني هو نقص إنزيم الغلوكوز-6-فوسفات ديهيدروجيناز (Glucose-6-Phosphate Dehydrogenase أو G6PD)، المعروف شعبياً بـ”التفوّل” أو “أنيميا الفول”. هذا النقص الوراثي المرتبط بالكروموسوم X شائع جداً في المنطقة العربية والشرق الأوسط؛ إذ تتراوح نسبة انتشاره في السعودية بين 2-7% حسب المنطقة الجغرافية. عند تعرض الرضيع المصاب بنقص G6PD لمحفزات معينة — بعض الأدوية، أو العدوى، أو حتى المواد الكيميائية في كرات النفثالين — تتكسر خلايا دمه بشراسة، ويرتفع البيليروبين بسرعة صاروخية.
هناك أيضاً أسباب أخرى تُسهم في هذه المعادلة الخطيرة. النزيف الداخلي أو الكدمات الواسعة التي تحدث في أثناء الولادة المتعسرة — مثل الورم الدموي الرأسي (Cephalohematoma) — تُشكّل مصدراً إضافياً ضخماً للبيليروبين عند تحلّل الدم المتجمع. كذلك، العدوى البكتيرية في الدم (Neonatal Sepsis) تزيد من تكسر خلايا الدم وتُضعف وظيفة الكبد في الوقت ذاته، مما يُنشئ عاصفة مثالية لارتفاع البيليروبين. ومن الأسباب النادرة لكنها مهمة: متلازمة كريغلر-نجار (Crigler-Najjar Syndrome)، وهي حالة وراثية يكون فيها إنزيم UGT1A1 غائباً تماماً أو شبه غائب، مما يعني أن الكبد عاجز بالكامل عن تحويل البيليروبين.
معلومة سريعة: أثبتت دراسة منشورة في مجلة Pediatrics عام 2022 أن نقص إنزيم G6PD يُعَدُّ عامل الخطر الأول لتطور اليرقان النووي في دول الشرق الأوسط وإفريقيا جنوب الصحراء، متقدماً على عدم توافق فصائل الدم. (Pediatrics, AAP)
من هم الأطفال الأكثر عرضة للإصابة باليرقان النووي؟
ليس كل رضيع مصاب بيرقان معرّض بالقدر نفسه لخطر تلف الدماغ بسبب اليرقان. هناك عوامل محددة ترفع الخطر بشكل ملموس، ومعرفتها تساعد الأهل والطبيب على اتخاذ قرارات استباقية.
الأطفال الخدج — المولودون قبل الأسبوع 37 من الحمل — يأتون في مقدمة القائمة. كبد الخديج أقل نضجاً بكثير، وحاجز الدم في دماغه أكثر هشاشة ونفاذية، ومستويات الألبومين لديه أقل. لهذا، فإن مستويات بيليروبين قد تكون “مقبولة” عند رضيع مكتمل الحمل يمكن أن تكون مميتة عند خديج. القاعدة الطبية تقول: كلما كان عمر الحمل أقل، كان عتبة التدخل أخفض.
صعوبات الرضاعة الطبيعية تمثل عامل خطر يُغفله كثيرون. حين لا يرضع الطفل بشكل كافٍ في الأيام الأولى، يتعرض للجفاف، وتقل حركة أمعائه، مما يبطئ التخلص من البيليروبين عبر البراز. أكثر من ذلك، يوجد آلية تُسمى الدورة المعوية الكبدية (Enterohepatic Circulation) يُعاد فيها امتصاص البيليروبين من الأمعاء إلى الدم إذا لم يُطرد مع البراز بسرعة كافية. الرضاعة الجيدة والمتكررة (8-12 مرة في اليوم) هي في الحقيقة أقوى سلاح وقائي طبيعي ضد ارتفاع البيليروبين عند حديثي الولادة.
العوامل الوراثية والتاريخ العائلي لها دور أيضاً. إذا كان لدى الأسرة طفل سابق عانى من يرقان شديد، أو إذا كان أحد الوالدين يحمل نقص G6PD، فإن الرضيع الجديد يحتاج مراقبة أكثر حزماً. كما أن الأطفال الذكور أكثر عرضة من الإناث لنقص G6PD لأنه مرتبط بالكروموسوم X. ومن عوامل الخطر الأخرى: وجود أخ أو أخت سابقين احتاجوا للعلاج الضوئي، والولادة بأدوات مساعدة (ملقط أو شفط) تسبب كدمات، ووجود كثرة كريات الدم الحمراء (Polycythemia) عند الرضيع.
| عامل الخطر | درجة الخطورة | آلية التأثير | ملاحظة سريرية |
|---|---|---|---|
| الولادة المبكرة (الخداج) | مرتفع جداً | كبد غير ناضج، حاجز دم-دماغ هش، ألبومين منخفض | عتبة التدخل أخفض بكثير من المكتمل |
| نقص إنزيم G6PD | مرتفع جداً | تكسر حاد لخلايا الدم الحمراء عند التعرض لمحفزات | شائع جداً في منطقة الخليج والشرق الأوسط |
| عدم توافق فصيلة الدم (Rh أو ABO) | مرتفع | أجسام مضادة من دم الأم تهاجم خلايا دم الرضيع | يتطلب فحص كومبز المباشر فوراً |
| صعوبات الرضاعة الطبيعية | متوسط | جفاف + بطء طرح البيليروبين + زيادة الدورة المعوية الكبدية | 8 إلى 12 رضعة يومياً تُقلل الخطر بشكل ملحوظ |
| كدمات ونزيف الولادة المتعسرة | متوسط | تحلل الدم المتجمع يُنتج بيليروبيناً إضافياً | الورم الدموي الرأسي من أبرز الأسباب |
| تاريخ عائلي لليرقان الشديد | متوسط | احتمال وراثة نقص G6PD أو عوامل أخرى | يستوجب مراقبة أكثر حزماً من البداية |
| العدوى البكتيرية (الإنتان الوليدي) | مرتفع | تكسر خلايا الدم + ضعف وظيفة الكبد معاً | عاصفة مثالية لارتفاع البيليروبين الكارثي |
| قصور الغدة الدرقية الخلقي | متوسط | إبطاء نضج إنزيمات الكبد بما فيها UGT1A1 | يُطيل مدة اليرقان ويزيد شدته |
الدكتور عبد الرحمن الصباغ — خبير طب الأطفال وحديثي الولادة في موقع وصفة طبية — يوصي كل أم بمراقبة عدد مرات الرضاعة وعدد الحفاضات المبللة والمتسخة يومياً في الأسبوع الأول: “إذا كان طفلك لا يبلل 6 حفاضات على الأقل يومياً بحلول اليوم الرابع، أو إذا لاحظتِ أن برازه لا يزال أسود (العقي) بعد اليوم الثالث، فهذه علامة على أنه لا يحصل على كفايته من الحليب — وهذا يرفع خطر تراكم البيليروبين. لا تنتظري، راجعي الطبيب أو اختصاصية الرضاعة فوراً.”
اقرأ أيضاً: المغص عند الأطفال الرضع: الأسباب الطبية وأفضل الطرق المجربة لتهدئة طفلك
كيف تتعرّف على أعراض اليرقان النووي قبل فوات الأوان؟
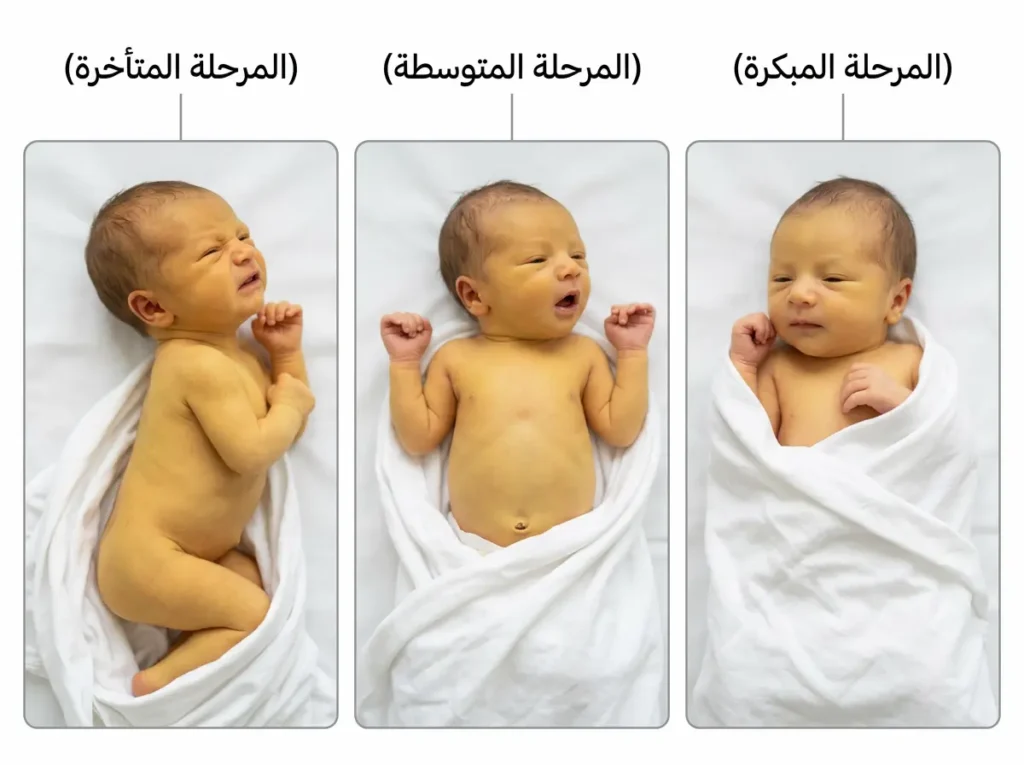
هنا الجزء الأهم في هذا المقال بأكمله. إن كنت ستحفظ شيئاً واحداً مما تقرأه، فليكن هذا القسم. اليرقان النووي لا يحدث فجأة — بل يمر بمراحل متصاعدة، ولكل مرحلة علاماتها التحذيرية. المصطلح الطبي الأدق للمرحلة التي تسبق التلف الدائم هو اعتلال الدماغ الحاد بالبيليروبين (Acute Bilirubin Encephalopathy أو ABE)، وهو يمثل نافذة الإنقاذ — اللحظات التي لا يزال فيها التدخل ممكناً.
المرحلة المبكرة هي المرحلة التي يمكن فيها إنقاذ الدماغ بالكامل إذا تصرفت بسرعة. العلامات تشمل: خمولاً شديداً يتجاوز “النعاس الطبيعي” — الطفل يصعب إيقاظه حتى للرضاعة. يرفض الثدي أو الزجاجة. نبرة بكائه تتغير وتصبح ضعيفة أو حادة. يبدو مرتخياً كالدمية القماشية (ضعف التوتر العضلي أو Hypotonia). هذه العلامات دقيقة وقد تبدو “عادية” لأم لأول مرة — لكنها ليست عادية أبداً.
المرحلة المتوسطة هي جرس الإنذار الأخير. الطفل يصبح مُهيَّجاً بشدة ولا يهدأ. بكاؤه يتحول إلى صراخ حاد عالي النبرة (High-pitched Cry) يختلف تماماً عن بكاء الجوع أو المغص. الأخطر هو ظهور وضعية التقوس: يقوّس الطفل ظهره ورقبته للخلف بشكل لا إرادي — وهذا ما يسميه الأطباء بوضعية تقوس الظهر (Opisthotonus) أو تقوس الرقبة (Retrocollis). هذه الوضعية ليست حركة عشوائية — بل هي علامة أن البيليروبين بدأ يؤذي جذع الدماغ فعلاً.
المرحلة المتأخرة هي مرحلة التلف الذي لا عودة منه. تظهر تشنجات عصبية حقيقية. قد يدخل الطفل في غيبوبة. العضلات تتصلب تصلباً كاملاً. في هذه المرحلة، حتى لو خفضنا البيليروبين، فإن الضرر الدماغي أصبح دائماً. ولهذا السبب أكرر: كل ساعة تأخير تُكلّف خلايا عصبية لا تتجدد.
هل تعلم؟ بحسب الأكاديمية الأميركية لطب الأطفال (AAP)، فإن الرضيع الذي يبلغ مستوى البيليروبين لديه 25 ملغ/ديسيلتر أو أكثر — مع وجود عامل خطر واحد على الأقل — يحتاج لنقل دم طارئ خلال ساعات، وليس أيام.
اقرأ أيضاً: الإسعافات الأولية: خطوات وإجراءات طبية تنقذ حياتك وقت الطوارئ
ما الذي يحدث حقاً داخل الدماغ؟ — المختبر الفسيولوجي للمهتمين بالتفاصيل العلمية الدقيقة
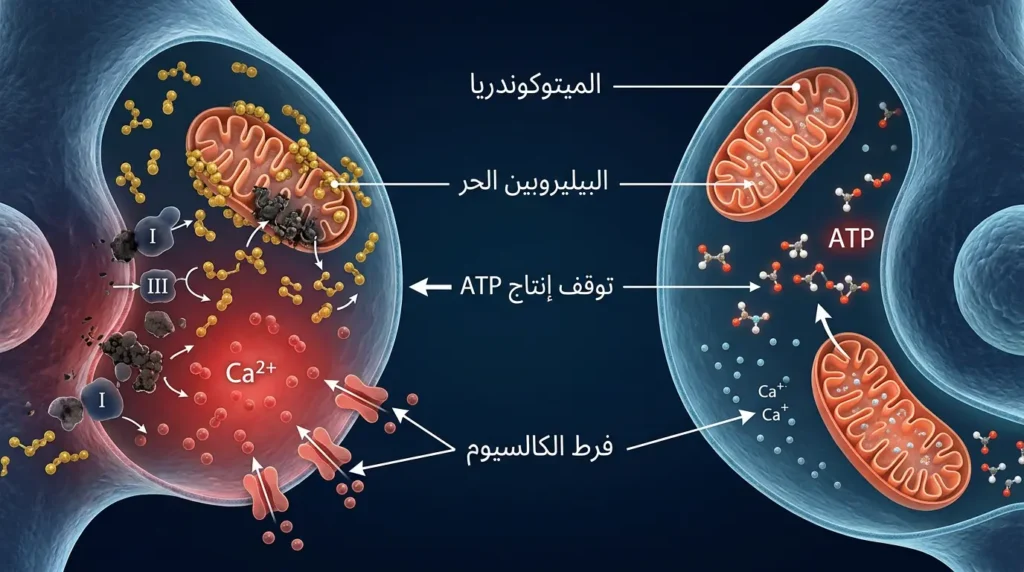
لمن يرغب في فهم الآلية العميقة لتلف الدماغ بسبب اليرقان، فإن القصة تبدأ على مستوى الجزيء. البيليروبين غير المقترن (Unconjugated Bilirubin أو UCB) ذائب في الدهون (Lipophilic)، وهذه الخاصية تمنحه القدرة على اختراق الأغشية الخلوية الغنية بالليبيدات، بما فيها أغشية الخلايا العصبية (Neurons) والخلايا الدبقية (Glial Cells). في الدورة الدموية الطبيعية، يرتبط معظم البيليروبين غير المقترن ببروتين الألبومين ارتباطاً وثيقاً، مما يحول دون عبوره لحاجز الدم في الدماغ. لكن حين يتجاوز تركيز البيليروبين سعة الارتباط بالألبومين — أو حين ينخفض مستوى الألبومين نفسه (كما يحدث عند الخدج أو المرضى) — يبقى جزء من البيليروبين حراً (Free Bilirubin أو Bf)، وهو الصورة الأكثر سُمّية.
عند دخوله إلى الخلايا العصبية، يتراكم البيليروبين في الميتوكوندريا ويعطّل سلسلة نقل الإلكترونات (Electron Transport Chain)، وبالتحديد المعقدات I وIII (Complex I & III). هذا يُوقف إنتاج الأدينوسين ثلاثي الفوسفات (ATP) — وقود الخلية — مما يدفع الخلية إلى الموت المبرمج (Apoptosis) أو النخر (Necrosis). بالإضافة إلى ذلك، يُحدث البيليروبين اضطراباً في توازن الكالسيوم داخل الخلية (Intracellular Calcium Homeostasis) عبر تنشيط مستقبلات NMDA الغلوتاماتية بإفراط، مما يؤدي إلى ظاهرة “السُّمّية الاستثارية” (Excitotoxicity) — وهي آلية تُدمّر فيها الخلية العصبية نفسها بنفسها بسبب فرط التنبيه.
لقد أظهرت أبحاث حديثة نُشرت في مجلة Seminars in Perinatology عام 2024 أن البيليروبين يُنشّط أيضاً مسارات الالتهاب العصبي (Neuroinflammation) عبر تحفيز الخلايا الدبقية الصغيرة (Microglia) لإطلاق السيتوكينات الالتهابية مثل TNF-α وIL-1β. هذا الالتهاب يُضاعف الضرر ويُوسّع رقعة التلف لتشمل مناطق لم يصلها البيليروبين مباشرة. الدماغ النامي — بأوعيته الدموية الهشة ونقص الميالين (Myelin) حول محاوره العصبية — يكون حساساً بشكل استثنائي لهذه الهجمة المزدوجة: السُّمّية المباشرة والالتهاب غير المباشر.
السبب في استهداف النوى القاعدية والكرة الشاحبة (Globus Pallidus) تحديداً يعود إلى غناها بالمستقبلات الغلوتاماتية ومعدل استهلاكها العالي للأكسجين والطاقة، مما يجعلها الأكثر هشاشةً أمام أي انقطاع في إنتاج ATP. من هنا تأتي الأعراض الحركية المميزة لليرقان النووي — وتحديداً الشلل الدماغي الكنعي (Athetoid Cerebral Palsy) — لأن هذه النوى هي المسؤولة عن التنسيق الحركي الدقيق والتحكم في الحركات اللاإرادية.
ومضة علمية: نوى السمع في جذع الدماغ (Auditory Nuclei) حساسة جداً للبيليروبين أيضاً، ولهذا فإن فقدان السمع الحسي العصبي (Sensorineural Hearing Loss) قد يكون العلامة الأولى — وأحياناً الوحيدة — لتلف دماغي بيليروبيني لم يُكتشف في الوقت المناسب.
كيف يشخّص الطبيب اليرقان النووي ويؤكده؟
التشخيص رحلة تبدأ بالعين المجردة وتنتهي بالتصوير الدماغي المتقدم. في الخطوة الأولى، يُجري الطبيب فحصاً سريرياً دقيقاً لتقييم مدى انتشار الاصفرار. القاعدة التقريبية المعروفة باسم “قاعدة كرامر” (Kramer’s Rule) تربط بين مناطق الاصفرار ومستوى البيليروبين: الاصفرار المقتصر على الوجه يقابل تقريباً 5-7 ملغ/ديسيلتر، بينما الاصفرار الذي يصل إلى الأطراف وراحة اليد يقابل مستويات تتجاوز 15-20 ملغ/ديسيلتر. لكن هذه القاعدة تقريبية وغير موثوقة بما يكفي — خصوصاً عند الأطفال ذوي البشرة الداكنة — ولذلك لا يُعتمد عليها وحدها أبداً.
الخطوة الحاسمة هي قياس مستوى البيليروبين الكلي في المصل (Total Serum Bilirubin أو TSB) عبر سحب عينة دم. يُقارن الرقم الناتج بمخططات بوتاني (Bhutani Nomogram) التي تُحدد مستوى الخطر بناءً على عمر الرضيع بالساعات وعوامل الخطر الموجودة. فقد أصبحت هذه المخططات — المنشورة أصلاً عام 1999 والمحدّثة عدة مرات — الأداة القياسية عالمياً لاتخاذ قرار بدء العلاج الضوئي أو نقل الدم. في كثير من المستشفيات السعودية الكبرى، يُستخدم أيضاً جهاز قياس البيليروبين عبر الجلد (Transcutaneous Bilirubinometer) كأداة فرز أولية سريعة لا تحتاج لوخز الطفل.
إلى جانب البيليروبين، يطلب الطبيب فحوصات مخبرية إضافية لتحديد سبب الارتفاع: تعداد الدم الكامل (CBC) مع عدد الخلايا الشبكية (Reticulocyte Count) لتقييم مدى تكسر الدم، فصيلة دم الأم والطفل مع اختبار كومبز المباشر (Direct Coombs Test) للكشف عن عدم التوافق المناعي، ومستوى G6PD، ومسحة الدم المحيطي (Peripheral Blood Smear) للبحث عن أشكال غير طبيعية لخلايا الدم الحمراء.
أما في حال الاشتباه بحدوث تلف دماغي فعلي، فإن التصوير بالرنين المغناطيسي (MRI) هو الفحص الأدق. يُظهر الرنين تغيرات مميزة في إشارة النوى القاعدية — وتحديداً الكرة الشاحبة (Globus Pallidus) — على تصوير T1 المرجح وT2 المرجح. هذه التغيرات قد لا تظهر إلا بعد عدة أيام من بداية الأعراض العصبية. فحص السمع عبر استجابة جذع الدماغ السمعية (Auditory Brainstem Response أو ABR) ضروري أيضاً للكشف المبكر عن تأثر نوى السمع، وهو من أولى المناطق تضرراً.
رقم لافت: وفقاً لبيانات برنامج فحص حديثي الولادة في السعودية، يتم إجراء أكثر من 500,000 فحص سمع لحديثي الولادة سنوياً في المملكة، ويُكتشف عبرها نسبة ملحوظة من حالات ضعف السمع المرتبط بفرط بيليروبين الدم.
ما هي خيارات العلاج العاجل لإنقاذ دماغ الطفل؟
⚠️ تحذير طبي: لا يجوز بأي حال من الأحوال تأخير العلاج الطبي لارتفاع البيليروبين الشديد أو استبداله بأي وصفات منزلية أو أعشاب. كل ساعة تأخير تعني خسارة خلايا عصبية لا تعوَّض. اذهبوا إلى أقرب طوارئ فوراً.
الهدف العلاجي واضح وصريح: خفض مستوى البيليروبين في الدم بأسرع ما يمكن قبل أن يلحق المزيد من الضرر بالدماغ. لا يوجد دواء يعالج الخلايا العصبية التالفة — العلاج كله وقائي بطبيعته.
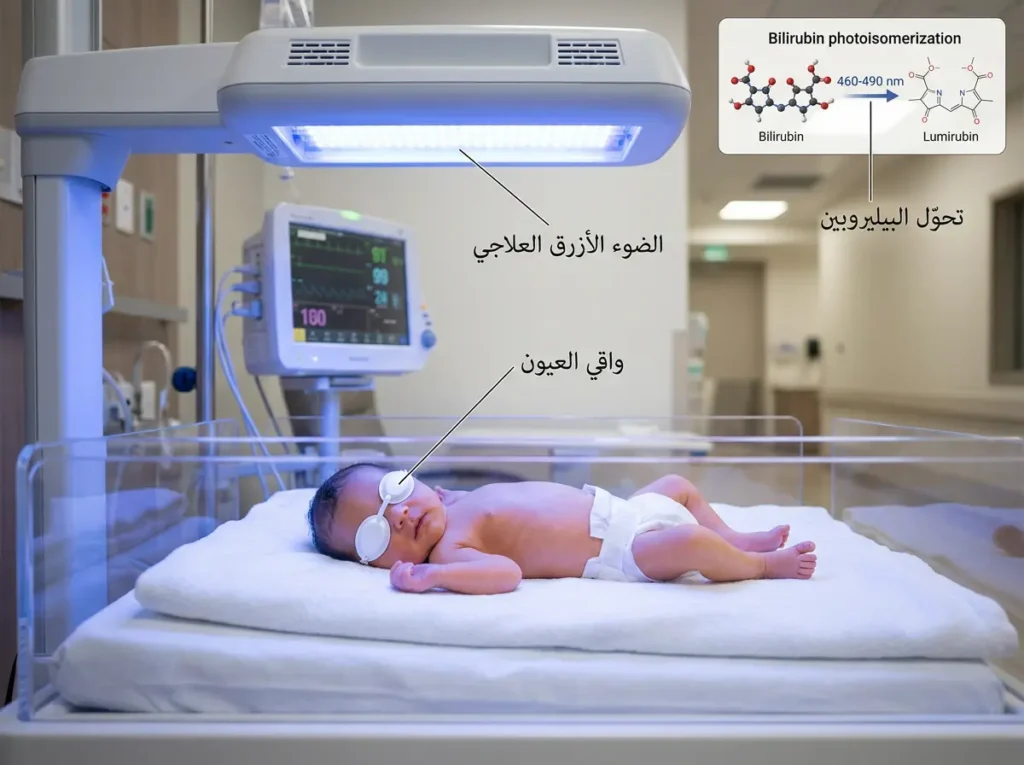
العلاج بالضوء المكثف (Intensive Phototherapy) هو خط الدفاع الأول وأكثر العلاجات استخداماً. الفكرة ببساطة: عندما تُسلَّط أشعة ضوئية ذات طول موجي محدد (عادةً 460-490 نانومتر، أي ضوء أزرق مائل للأخضر) على جلد الرضيع العاري، فإنها تخترق الجلد وتصل إلى البيليروبين غير المقترن في الشعيرات الدموية السطحية وتُحدث فيه تحولاً كيميائياً يسمى “التماكب الضوئي” (Photoisomerization). هذا التحول ينتج أشكالاً من البيليروبين — أهمها اللوميبيليروبين (Lumirubin) — قابلة للذوبان في الماء ويمكن طرحها مباشرة عبر الكلى والصفراء دون الحاجة لتحويل كبدي.
يُشير المستشار الدوائي جاسم محمد مراد — خبير الصحة والإمداد الطبي في موقع وصفة طبية — إلى أن فعالية العلاج الضوئي تعتمد على ثلاثة عوامل أساسية: “شدة الإشاعة الضوئية (يجب أن تكون 30 ميكروواط/سم²/نانومتر على الأقل للعلاج المكثف)، ومساحة الجلد المكشوفة (كلما كان الطفل مكشوفاً أكثر مع حماية العينين والأعضاء التناسلية كان العلاج أسرع)، والمسافة بين مصدر الضوء وجلد الطفل (كلما كانت المسافة أقرب كانت الشدة أعلى). أجهزة LED الحديثة المستخدمة في المستشفيات السعودية حالياً أكثر كفاءةً وأقل حرارةً من الأجهزة القديمة.”
في أثناء العلاج الضوئي، يحتاج الطفل للتغذية المستمرة (رضاعة طبيعية أو صناعية كل 2-3 ساعات) للحفاظ على الترطيب وتنشيط حركة الأمعاء وطرد البيليروبين. قد يحتاج بعض الرضع لسوائل وريدية إضافية إذا كانت التغذية الفموية غير كافية أو إذا كان الجفاف شديداً.
نقل وتغيير الدم (Exchange Transfusion) هو الحل الطارئ حين يفشل العلاج الضوئي المكثف أو حين تكون مستويات البيليروبين مرتفعة بشكل كارثي (عادةً فوق 25 ملغ/ديسيلتر عند رضيع مكتمل الحمل مع عوامل خطر، أو حين تظهر علامات اعتلال الدماغ). في هذا الإجراء، يُسحب دم الطفل تدريجياً عبر قسطرة في الحبل السري ويُستبدل بدم متبرع طازج. كل دورة تُزيل نسبة كبيرة من البيليروبين والأجسام المضادة المهاجمة لخلايا الدم. الإجراء يتم في وحدة العناية المركزة لحديثي الولادة (NICU) تحت مراقبة مستمرة للقلب والتنفس ومستويات السكر والكالسيوم والبوتاسيوم في الدم. المضاعفات المحتملة تشمل: انخفاض مستوى الكالسيوم، واضطرابات نظم القلب، وخطر العدوى، والتهاب الأمعاء النخري (NEC) — لكنها نادرة في الأيدي الخبيرة، والفائدة تفوق الخطر حين تكون حياة الدماغ على المحك.
من العلاجات المساعدة التي برزت في السنوات الأخيرة: استخدام الغلوبيولين المناعي الوريدي (Intravenous Immunoglobulin أو IVIG) في حالات عدم التوافق المناعي (Rh أو ABO)؛ إذ يُبطئ تدمير خلايا الدم الحمراء ويُقلل الحاجة لنقل الدم. جرعته المعتادة هي 0.5-1 غ/كغ تُعطى وريدياً على مدى ساعتين، ويمكن تكرارها مرة واحدة بعد 12 ساعة إذا استمر البيليروبين في الارتفاع. لقد أثبتت مراجعة كوكرين (Cochrane Review) عام 2018 أن IVIG يُقلل بشكل ملحوظ من حاجة الرضع لنقل الدم في حالات عدم التوافق المناعي.
من المثير أن تعرف: هناك دواء واعد يُسمى ستانات القصدير (Tin Mesoporphyrin أو SnMP) يعمل عن طريق تثبيط إنزيم هيم أوكسيجيناز (Heme Oxygenase) المسؤول عن إنتاج البيليروبين من الهيم. تجارب سريرية في مراحل متقدمة (حتى عام 2025) أظهرت نتائج مشجعة في خفض البيليروبين عند حديثي الولادة عاليي الخطورة، لكنه لم يحصل بعد على موافقة إدارة الغذاء والدواء الأميركية (FDA) للاستخدام الروتيني.
| وجه المقارنة | العلاج الضوئي | نقل وتغيير الدم |
|---|---|---|
| طبيعة الإجراء | غير جراحي — تعريض الجلد للضوء الأزرق | إجراء طبي جراحي يتم عبر قسطرة في الحبل السري |
| آلية العمل | تحويل البيليروبين إلى لوميبيليروبين قابل للطرح عبر البول | إزالة البيليروبين والأجسام المضادة مباشرةً من الدم باستبداله بدم متبرع |
| متى يُستخدم | الخط الأول عند ارتفاع البيليروبين فوق عتبة التدخل | فشل العلاج الضوئي أو بيليروبين فوق 25 ملغ/ديسيلتر مع عوامل خطر |
| سرعة خفض البيليروبين | تدريجية — خلال ساعات إلى أيام | سريعة جداً — خلال ساعات قليلة |
| مكان الإجراء | وحدة مواليد أو حضّانة عادية | وحدة العناية المركزة لحديثي الولادة (NICU) حصراً |
| المتطلبات الأساسية | جهاز LED أزرق، واقي عيون، ترطيب كافٍ | دم متبرع متوافق، فريق متخصص، مراقبة مستمرة للقلب والكيمياء |
| المخاطر الرئيسة | فقدان سوائل خفيف، طفح جلدي عابر | انخفاض كالسيوم، اضطراب نظم القلب، خطر عدوى نادر |
| التكلفة التقريبية بالسعودية | 1,500 إلى 4,000 ريال في المستشفيات الخاصة | 15,000 إلى 40,000 ريال شاملةً العناية المركزة |
| التغذية خلال الإجراء | مستمرة — رضاعة كل 2 إلى 3 ساعات ضرورية | موقوفة مؤقتاً خلال الإجراء، تستأنف بعده |
ما هي المضاعفات التي يتركها اليرقان النووي على حياة الطفل؟
حين يتجاوز البيليروبين نقطة اللاعودة ويُتلف النوى الدماغية، فإن الآثار تكون دائمة ومتعددة الأبعاد. ليس هناك “شفاء” من اليرقان النووي بعد حدوث التلف — كل ما يمكن فعله هو إعادة التأهيل والعلاج الداعم لتحسين جودة حياة الطفل.
الشلل الدماغي الكنعي (Athetoid أو Dyskinetic Cerebral Palsy) هو أشهر وأوضح مضاعفات اليرقان النووي. يتميز بحركات لاإرادية بطيئة ومتلوية في الأطراف والوجه واللسان، مع صعوبة في التحكم بالوضعية والتوازن. هذه الحركات تزداد سوءاً مع الإجهاد والانفعال وتهدأ في أثناء النوم. السبب هو تلف الكرة الشاحبة والنواة تحت المهادية (Subthalamic Nucleus) المسؤولتين عن تنسيق الحركات وتثبيط الحركات غير المرغوبة.
فقدان السمع الحسي العصبي (Sensorineural Hearing Loss) أو اضطراب طيف الاعتلال العصبي السمعي (Auditory Neuropathy Spectrum Disorder أو ANSD) يصيب نسبة كبيرة من الناجين. وقد يتراوح من ضعف سمع خفيف إلى صمم كامل. المميز في هذا النوع من فقدان السمع أنه يؤثر بشكل خاص على القدرة على تمييز الكلام وسط الضوضاء — أي أن الطفل قد “يسمع” الأصوات لكنه لا يفهم الكلمات — لأن المشكلة في العصب وليس في الأذن الداخلية نفسها.
مشاكل التطور الحركي والعقلي تظهر تدريجياً مع نمو الطفل. قد يتأخر في الجلوس والمشي والكلام. في بعض الحالات يحافظ الطفل على ذكاء طبيعي أو قريب من الطبيعي رغم الإعاقة الحركية — وهذا ما يجعل التشخيص الدقيق والتأهيل المبكر بالغَي الأهمية. مشاكل أخرى تشمل: تشوهات في مينا الأسنان الدائمة (تبدو خضراء أو بنية مصفرة)، واضطرابات في حركة العين وبخاصة صعوبة النظر للأعلى بسبب شلل نظر عمودي (Vertical Gaze Palsy) ناتج عن تلف نوى الأعصاب المحركة للعين في جذع الدماغ.
صندوق اقتباس طبي:
وفقاً لتقرير منظمة الصحة العالمية (WHO) الصادر عام 2023 حول “صحة حديثي الولادة”، فإن اليرقان الشديد يمثل واحداً من أكثر الأسباب التي يمكن الوقاية منها لإعاقة الأطفال في البلدان ذات الدخل المنخفض والمتوسط، ويتسبب في إعاقة دائمة لنحو 178,000 طفل سنوياً على مستوى العالم.
اقرأ أيضاً:
- تأخر الكلام واللغة عند الأطفال: الأسباب الطبية والعلامات التحذيرية وأحدث طرق العلاج
- تأخر ظهور الأسنان عند الأطفال: متى تقلق وما هي الأسباب الحقيقية؟
ما بعد الصدمة: كيف تتعايش الأسرة مع تشخيص اليرقان النووي؟
عندما يؤكد الأطباء حدوث تلف دماغي دائم للطفل، تدخل الأسرة في نفق مظلم من الشعور بالذنب، والصدمة، والأسئلة التي لا تنتهي عن “ماذا لو تصرفنا أبكر؟”. هذا العبء النفسي هائل، ومواجهته تتطلب شجاعة استثنائية ودعماً لا محدوداً. الخطوة الأولى للتعافي الأسري هي التوقف الفوري عن لوم الذات أو تبادل الاتهامات بين الزوجين؛ فاليرقان النووي يتطور أحياناً بشراسة وسرعة قد تخدع حتى بعض الممارسين الصحيين غير المتمرسين. توجيه الطاقة نحو دعم الطفل هو الخيار الوحيد والأكثر جدوى.
الاندماج المبكر في برامج التدخل المبكر ليس مجرد رفاهية طبية، بل هو إعادة صياغة لمستقبل الطفل. بالتوازي مع ذلك، يحتاج الآباء والأمهات إلى الانضمام لمجموعات الدعم النفسي (Support Groups) التي تضم أسراً تمر بنفس التحديات. سماع تجارب الآخرين ورؤية أطفال كبروا وتجاوزوا الكثير من إعاقاتهم الحركية عبر العلاج الطبيعي يمنح طاقة أمل لا تُقدر بثمن. تذكروا دائماً أن الإعاقة الحركية أو السمعية لا تعني بالضرورة غياب الذكاء أو القدرة على الإبداع؛ فكثير من الأطفال الناجين من اليرقان النووي يمتلكون قدرات إدراكية ممتازة تنتظر فقط من يكتشفها ويوفر لها أدوات التواصل المناسبة.
كيف تحمي طفلك قبل أن تبدأ المشكلة؟
خط الدفاع الأول ضد اليرقان النووي ليس العلاج — بل الوقاية. وهذه الوقاية ليست معقدة ولا تحتاج تكنولوجيا متقدمة. تحتاج فقط إلى: وعي، ومتابعة، وعدم تأجيل.
التغذية المبكرة والكافية هي حجر الأساس. الرضاعة الطبيعية المتكررة — كل 1.5 إلى 3 ساعات في الأيام الأولى — تُنشّط حركة أمعاء الرضيع وتُساعد على طرد العقي (Meconium) المحمّل بالبيليروبين. كلما أخرج الطفل برازاً أكثر، قلّ البيليروبين المُعاد امتصاصه من الأمعاء. إذا كانت الرضاعة الطبيعية صعبة في البداية — وهذا شائع ولا يُعيب — فلا تترددي في طلب المساعدة من اختصاصية الرضاعة (Lactation Consultant) أو إضافة حليب صناعي مؤقتاً بتوجيه الطبيب لضمان حصول الطفل على كفايته من السوائل.
الالتزام بموعد المراجعة الطبية خلال 24-48 ساعة من الخروج من المستشفى أمر غير قابل للتفاوض. كثير من حالات اليرقان النووي في السعودية والعالم العربي حدثت لأن الأسرة لم تراجع الطبيب في الموعد المحدد بعد الخروج. هذا الموعد ليس “إجراءً روتينياً” — بل هو الفرصة الذهبية لاكتشاف ارتفاع البيليروبين قبل أن يصل إلى مستويات خطرة.
مراقبة لون الطفل بشكل صحيح تعني أن تفحصي لونه في ضوء النهار الطبيعي (بجانب النافذة)، وليس تحت إضاءة الغرفة الصفراء. اضغطي برفق على جبهة الطفل أو صدره بإصبعك ثم ارفعي إصبعك: إذا كان الجلد تحتها أصفر اللون وليس ورديّاً، فهذه علامة يرقان. إذا وصل الاصفرار إلى بطنه أو ساقَيه أو باطن قدمَيه — فهذا يستدعي مراجعة فورية.
حقيقة طبية: أظهرت دراسة نُشرت في Journal of Tropical Pediatrics عام 2023 أن التثقيف الصحي للأمهات قبل الولادة حول علامات اليرقان الخطير أدى إلى انخفاض بنسبة 40% في حالات التأخر في طلب الرعاية الطبية لارتفاع البيليروبين الشديد في مراكز الرعاية الأولية.
ما بين الخرافة والحقيقة: أخطر المعتقدات الشائعة عن صفار المواليد
❌ الخرافة: تعريض الطفل لأشعة الشمس المباشرة عبر النافذة يُغني عن العلاج الضوئي في المستشفى.
✅ الحقيقة: ضوء الشمس غير المباشر يحتوي على بعض الأطوال الموجية المفيدة، لكن شدته أضعف بمراحل من أجهزة العلاج الضوئي الطبية. كما أن التعرض المباشر للشمس يُعرّض الرضيع لخطر ضربة الشمس والحروق الجلدية وعدم استقرار حرارة الجسم. الأكاديمية الأميركية لطب الأطفال لا توصي بتشميس المواليد كعلاج لليرقان. لا يمكن لأي شمس أن تحل محل جهاز علاج ضوئي بشدة 30 ميكروواط/سم²/نانومتر.
❌ الخرافة: إعطاء الرضيع ماء أو ماء سكر يُساعد في “تنظيف الجسم” من الصفار.
✅ الحقيقة: الماء والسكر لا يُخفّضان البيليروبين، بل قد يُسببان نقصاً في الصوديوم (Hyponatremia) أو يُقلّلان من رغبة الطفل في الرضاعة، مما يزيد الأمر سوءاً. أفضل سائل يمكن أن يحصل عليه الرضيع هو حليب الأم أو الحليب الصناعي المخصص لعمره.
❌ الخرافة: اليرقان مرض يصيب الأطفال فقط ولا يمكن أن يسبب مشاكل دائمة.
✅ الحقيقة: اليرقان نفسه ليس دائماً خطيراً — لكن ارتفاع البيليروبين إلى مستويات سُمّية دون علاج يسبب تلفاً دماغياً لا رجعة فيه. والسؤال “هل اليرقان يسبب تخلفاً عقلياً أو تلفاً بالدماغ” — الجواب: نعم، إذا وصل إلى مرحلة اليرقان النووي.
❌ الخرافة: إذا كان الطفل يرضع جيداً ونشيطاً، فلا داعي للقلق من أي اصفرار.
✅ الحقيقة: في المراحل المبكرة جداً من ارتفاع البيليروبين، قد يبدو الطفل طبيعياً تماماً. العلامات العصبية لا تظهر إلا عندما يكون البيليروبين مرتفعاً بشدة. الاعتماد على “مظهر الطفل” وحده دون قياس مستوى البيليروبين يُعَدُّ خطأً طبياً.
❌ الخرافة: العلاج بالضوء يُتلف عيون الطفل أو جلده.
✅ الحقيقة: عيون الطفل تُغطّى دائماً بواقٍ خاص في أثناء العلاج الضوئي. الجلد قد يُظهر طفحاً عابراً أو زيادة في فقدان السوائل عبر التعرق، لكن هذه آثار بسيطة وقابلة للسيطرة. الأضرار المحتملة من العلاج الضوئي لا تُقارن إطلاقاً بالتلف الدماغي الذي يمنعه.
هل يُشير اليرقان الشديد إلى مشكلات صحية أخرى في جسم الرضيع؟
اليرقان ليس مرضاً بذاته دائماً — بل قد يكون عَرَضاً لمشكلة أعمق. والطبيب الذي يعالج الاصفرار دون البحث عن سببه يُشبه من يُطفئ إنذار الحريق دون أن يبحث عن مصدر الدخان.
عدم توافق فصائل الدم بين الأم والطفل (Hemolytic Disease of the Newborn) — سواء عدم توافق Rh أو ABO — هو مرض مناعي ذاتي نقلي يستهدف خلايا دم الرضيع ويتطلب متابعة مناعية ودموية مستمرة. نقص إنزيم G6PD هو حالة وراثية مزمنة ستبقى مع الطفل مدى الحياة، وتستوجب تجنب قائمة محددة من الأدوية والأطعمة والمواد الكيميائية (كالفول، والأسبرين، ومركبات السلفا، والنفثالين). اكتشاف نقص G6PD في سياق يرقان حديثي الولادة يُعَدُّ “فرصة تشخيصية” ثمينة تُنقذ الطفل من نوبات تكسر دم مستقبلية.
العدوى البكتيرية الشاملة (Neonatal Sepsis) هي حالة طبية طارئة تتطلب مضادات حيوية وريدية فورية. اليرقان قد يكون العلامة الأولى التي تقود إلى اكتشاف العدوى. ومن الأمراض الأقل شيوعاً التي يكشفها اليرقان: قصور الغدة الدرقية الخلقي (Congenital Hypothyroidism) الذي يُبطئ نضج الكبد ويُطيل مدة اليرقان. وكذلك أمراض الاستقلاب الوراثية (Inborn Errors of Metabolism) مثل الغالاكتوزيميا (Galactosemia) التي تُلحق ضرراً بالكبد وتؤثر على قدرته على معالجة البيليروبين. فحص حديثي الولادة الموسع (Expanded Newborn Screening أو ENS) المطبق في السعودية منذ تحديثه عام 2023 يشمل الكشف عن G6PD وقصور الدرقية — اطمئني أن طفلك أجرى هذا الفحص.
معلومة سريعة: رقعة الفحص الورقية (Guthrie Card) التي تُؤخذ من كعب الرضيع بعد 48-72 ساعة من الولادة تفحص أكثر من 17 مرضاً في برنامج الفحص السعودي الحالي — بما فيها أمراض قد تُسبب يرقاناً مطوّلاً. لا تتأخري عن إجراء هذا الفحص لطفلك.
اقرأ أيضاً: جدول لقاحات الأطفال الروتينية: المواعيد الدقيقة، الآثار الجانبية، وأهم النصائح للأمهات
ما الذي يحدث للأم الحامل والمرضع: المسموح والممنوع لحماية المولود من اليرقان؟
⚠️ تنبيه طبي مهم: أي قرار بشأن الأدوية أو المكملات خلال الحمل والرضاعة يجب أن يتم بالتنسيق التام مع طبيب التوليد وطبيب الأطفال. لا تتوقفي عن أي دواء ولا تبدئي بأخذ أي مكمّل من تلقاء نفسك.
من جهة الوقاية قبل الولادة، فإن الخطوة الأهم هي إجراء فحص فصيلة الدم وعامل Rh للأم في الزيارات الأولى لمتابعة الحمل. إذا كانت الأم Rh سالبة، فستتلقى حقنة الغلوبيولين المناعي المضاد لـ D (Anti-D أو RhoGAM) في الأسبوع 28 من الحمل وبعد الولادة مباشرةً إذا كان الطفل Rh موجباً. هذه الحقنة تمنع تكوين أجسام مضادة في دم الأم قد تهاجم خلايا دم المولود التالي — وهي آمنة تماماً ولا تؤثر على الرضاعة.
أما بخصوص الأدوية التي تتناولها الأم: بعض الأدوية تعبر المشيمة وتتنافس مع البيليروبين على مواقع الارتباط بالألبومين في دم الرضيع، مما يزيد نسبة البيليروبين الحر السام. من أبرز هذه الأدوية: السلفوناميدات (Sulfonamides)، والسيفترياكسون (Ceftriaxone) بجرعات عالية. يجب على الطبيب تجنب وصفها قبل الولادة مباشرة أو للأم المرضع إلا عند الضرورة القصوى وبتقييم دقيق للمخاطر والفوائد.
بالنسبة للمكملات العشبية في أثناء الرضاعة: بعض الأمهات يتناولن الحلبة (Trigonella foenum-graecum) لزيادة إدرار الحليب. لا يوجد دليل علمي قوي على أن الحلبة بجرعاتها المعتادة ترفع البيليروبين عند الرضيع، لكنها قد تسبب نقصاً في مستوى السكر عند الأم أو الرضيع (Hypoglycemia) إذا أُخذت بكميات كبيرة. تجنبي الجرعات العالية المركّزة من مكملات الحلبة أثناء الأسابيع الأولى بعد الولادة، واكتفي بإضافتها كتوابل طبخ إن أحببتِ. أما الكركم (Curcuma longa) والزنجبيل (Zingiber officinale) فكلاهما آمن بكميات الطبخ العادية، لكن المكملات المركّزة منهما قد تؤثر على إنزيمات الكبد لدى الأم. إذا كانت الأم تتناول أي دواء لسيولة الدم بعد الولادة القيصرية (مثل الإينوكسابارين Enoxaparin)، فيجب عدم تناول مكملات الكركم المركّزة لأن الكركمين (المادة الفعّالة) يزيد من تأثير مضادات التخثر ويرفع خطر النزيف. استشيري الصيدلي السريري أو الطبيب قبل أي مكمّل.
الدكتورة نور الهدى القباني — طبيبة نسائية وتوليد وخبيرة الصحة الإنجابية في موقع وصفة طبية — تُشدّد على ضرورة إعلام طبيب الأطفال بأي دواء أو مكمّل تناولته الأم في الأسابيع الأخيرة من الحمل أو تتناوله في أثناء الرضاعة: “قائمة الأدوية الكاملة للأم هي جزء أساسي من تقييم يرقان المولود. لا تخجلي أبداً من ذكر أي مكمل أو عشبة لطبيبك.”
اقرأ أيضاً: سكري الحمل: الأسباب والأعراض وطرق السيطرة الفعالة لولادة آمنة
كم تكلّف علاجات اليرقان الشديد في المستشفيات؟
الحديث عن التكلفة أمر واقعي وضروري لأن كثيراً من الأسر تتردد في الذهاب للمستشفى خوفاً من الفواتير — وهذا التردد قد يُكلّف ما هو أغلى بكثير من المال.
العلاج بالضوء (Phototherapy): في المستشفيات الحكومية السعودية، يُقدَّم مجاناً ضمن التأمين الصحي الوطني أو تغطية وزارة الصحة. في المستشفيات الخاصة بالسعودية، تتراوح تكلفة الإقامة مع العلاج الضوئي بين 1,500-4,000 ريال سعودي (400-1,100 دولار أميركي تقريباً)، اعتماداً على مستوى المستشفى وطول مدة العلاج. عالمياً، في الولايات المتحدة، قد تتراوح تكلفة العلاج الضوئي مع الإقامة بين 2,000-5,000 دولار لليلة.
نقل وتغيير الدم (Exchange Transfusion): هو إجراء أعقد ويتم في وحدة العناية المركزة. تكلفته في المستشفيات الخاصة بالسعودية قد تصل إلى 15,000-40,000 ريال سعودي (4,000-10,700 دولار) شاملةً مشتقات الدم والمراقبة المركزة. في الولايات المتحدة، قد تتجاوز 15,000-20,000 دولار.
العوامل التي تتحكم في التكلفة تشمل: مدة الإقامة في الحضّانة، والحاجة لنقل الدم من عدمها، ونوع المستشفى (حكومي أو خاص)، ووجود مضاعفات مصاحبة، والحاجة لتصوير بالرنين المغناطيسي أو فحوصات سمعية متقدمة.
لكن الأهم من كل هذه الأرقام: تكلفة علاج مضاعفات اليرقان النووي الدائمة — من علاج طبيعي مدى الحياة، وسمّاعات أذن، وبرامج تأهيل حركي وسلوكي — تتجاوز مئات الآلاف على مدار عمر الطفل. الوقاية والعلاج المبكر هما أرخص استثمار صحي يمكنك القيام به.
كيف تتعاملين عملياً مع اليرقان خطوة بخطوة؟
- في المستشفى بعد الولادة مباشرةً: تأكدي أن طفلك أجرى فحص البيليروبين (عبر الجلد أو الدم) قبل الخروج. اسألي عن فصيلة دم الطفل وعن نتيجة اختبار كومبز.
- خلال أول 48 ساعة في المنزل: أرضعي طفلك كل 2-3 ساعات. لا تنتظري أن يبكي. أيقظيه للرضاعة إن نام أكثر من 3 ساعات.
- مراقبة اللون يومياً: افحصي لون طفلك بجوار النافذة في ضوء النهار. اضغطي برفق على جبهته وأنفه. لاحظي: هل الاصفرار يزداد يوماً بعد يوم؟ هل وصل إلى بطنه أو ساقَيه؟
- راقبي الحفاضات: الطفل الذي يرضع جيداً يبلل 6 حفاضات على الأقل يومياً بحلول اليوم الرابع، ويُخرج 3-4 مرات براز أصفر (لا أسود).
- علامات الطوارئ — اذهبي فوراً: بكاء حاد غير عادي، رفض تام للرضاعة، خمول شديد أو صعوبة في إيقاظ الطفل، تقوّس الظهر أو الرقبة للخلف، تشنجات، أو اصفرار شديد وصل إلى راحتَي اليدين أو باطن القدمين.
- موعد المراجعة: لا تُلغي أو تؤجّلي موعد المتابعة الطبية بعد 24-48 ساعة من الخروج. حتى لو بدا طفلك بخير.
- احتفظي بهذا الرقم: رقم الطوارئ في المستشفى الذي ولدتِ فيه، ورقم طبيب الأطفال الخاص.
- لا تعتمدي على الإنترنت أو نصائح الجيران: إذا شعرتِ بأي شك، اتصلي بالطبيب. الطبيب لن ينزعج من مكالمة احترازية. لكنه سيحزن كثيراً إذا جاء الطفل متأخراً.
نقطة تستحق الانتباه: في السعودية، تُوفّر خدمة “صحة 937” استشارات هاتفية مجانية على مدار الساعة من وزارة الصحة. إذا كنتِ في شك حول لون طفلك أو سلوكه ولا تستطيعين الوصول للمستشفى فوراً، اتصلي بهذا الرقم كخطوة أولى.
اقرأ أيضاً:
- صندوق الإسعافات الأولية: كيف تنقذ حياة من تحب في اللحظات الحرجة؟
- قواعد السلامة في المنزل: كيف تحمي عائلتك من المخاطر الخفية وتتجنب الكوارث
هل يمكن للعلاج أن يصلح ما أتلفه اليرقان النووي في الدماغ؟
لنكن صادقين: لا يوجد حتى اليوم علاج يستطيع إعادة بناء الخلايا العصبية التي دمّرها البيليروبين. الأبحاث في مجال الخلايا الجذعية (Stem Cell Therapy) والتحفيز الدماغي (Deep Brain Stimulation أو DBS) لا تزال في مراحلها التجريبية بالنسبة لتلف البيليروبين. ما يمكن فعله — ويجب فعله بكل جدية — هو التأهيل المبكر والمكثف لتحسين قدرات الطفل وتعظيم إمكاناته.
العلاج الطبيعي والوظيفي (Physical & Occupational Therapy) يبدأ في الأشهر الأولى من العمر ويستمر سنوات. يُركّز على تحسين التحكم بالرأس، والجلوس، والمشي، والمهارات اليدوية الدقيقة. العلاج النطقي (Speech-Language Therapy) ضروري للأطفال الذين يعانون من مشاكل في النطق أو البلع. السمّاعات الطبية أو زراعة القوقعة (Cochlear Implant) تُقرّر بناءً على شدة فقدان السمع ونوعه — مع ملاحظة أن اعتلال العصب السمعي الناجم عن البيليروبين لا يستجيب دائماً لزراعة القوقعة بنفس فعالية الصمم الناجم عن أسباب أخرى.
الدكتور أسامة محمد العظم — اختصاصي طب الأعصاب بخبرة 15 عاماً في موقع وصفة طبية — يؤكد أن “التدخل التأهيلي المبكر خلال السنتين الأوليين من العمر — حين يكون الدماغ في أقصى مرونته العصبية (Neuroplasticity) — يُحدث فرقاً جوهرياً في مستقبل الطفل. الدماغ الصغير يملك قدرة مدهشة على إعادة توزيع الوظائف إلى مناطق سليمة، لكن هذه النافذة لا تبقى مفتوحة إلى الأبد.”
اقرأ أيضاً: السكتة الدماغية: الأعراض التحذيرية المبكرة، الأسباب، وأحدث طرق العلاج والتعافي
الوصفة الطبية من موقعنا
هذه الوصفة ليست بديلاً عن العلاج الطبي لارتفاع البيليروبين — بل هي مكمّل وقائي يعزز قدرة جسم الرضيع على التعامل مع البيليروبين بكفاءة، وتوصيات للأم لدعم صحة مولودها:
- تكثيف الرضاعة في الساعات الأولى: البدء بالرضاعة خلال أول ساعة بعد الولادة (الساعة الذهبية) يُحفّز إفراز هرمون الأوكسيتوسين (Oxytocin) الذي يُسرّع نزول اللبأ (Colostrum). اللبأ غني بالأجسام المناعية ويعمل كملين طبيعي يساعد الرضيع على إخراج العقي سريعاً — وكل إخراج للعقي يعني تقليل كمية البيليروبين المعاد امتصاصها عبر الدورة المعوية الكبدية.
- ملامسة الجلد للجلد (Skin-to-Skin Contact): وضع الرضيع عارياً على صدر الأم يُنظّم جهازه العصبي الذاتي (Autonomic Nervous System)، ويُحسّن استقرار حرارة الجسم، ويُعزز نجاح الرضاعة. دراسات حديثة نشرت في Neonatology عام 2024 أظهرت أن ملامسة الجلد المبكرة والمتكررة ترتبط بانخفاض ملحوظ في ذروة مستويات البيليروبين خلال الأسبوع الأول.
- تغذية الأم المرضع بأطعمة غنية بالألبومين: الألبومين في دم الرضيع يعتمد جزئياً على تغذية الأم. البروتينات عالية القيمة البيولوجية (البيض، اللحوم، البقوليات) تُساعد في الحفاظ على مستوى كافٍ من الألبومين الذي يحمل البيليروبين بأمان في الدورة الدموية.
الدكتورة علا الأحمد — اختصاصية التغذية العلاجية في موقع وصفة طبية — توصي الأم المرضع في الأسبوع الأول بعد الولادة بتناول “وجبة غنية بالبروتين مع كل رضعة — حتى لو كانت حفنة مكسرات أو بيضة مسلوقة — لأن إنتاج الحليب يستهلك بروتيناً كبيراً، وأي نقص بروتيني عند الأم ينعكس على جودة الحليب وعلى مستويات الألبومين عند الرضيع.”
- تنظيم إيقاع النوم واليقظة عند الرضيع: تعريض الرضيع لضوء نهاري معتدل (غير مباشر) في أثناء ساعات النهار وتقليل الإضاءة ليلاً يساعد في ضبط الإيقاع اليوماوي (Circadian Rhythm) الذي يؤثر على نضج إنزيمات الكبد — بما فيها UGT1A1. هذه العلاقة مدعومة بأدلة ناشئة وليست قاطعة بعد، لكنها منطقية فسيولوجياً.
- تجنّب المواد الكيميائية المؤكسدة في بيئة الطفل: كرات النفثالين (Mothballs)، والحناء المحتوية على مواد كيميائية مضافة (خصوصاً الحناء السوداء)، وبعض المنظفات العطرية القوية — كلها قد تُحفّز تكسر الدم عند الأطفال المصابين بنقص G6PD (حتى لو لم يكن التشخيص معروفاً بعد). في الأسبوعين الأولين، أبعدي هذه المواد عن غرفة الرضيع تماماً.
- عدم تأجيل فحص السمع: حتى لو بدا طفلك يسمع ويستجيب للأصوات، فإن الاعتلال العصبي السمعي الخفيف قد لا يُلاحظ سريرياً. اطلبي فحص ABR (الاستجابة السمعية لجذع الدماغ) وليس فقط فحص OAE (الانبعاث السمعي الأذني)، خصوصاً إذا كان طفلك قد عانى من يرقان شديد أو احتاج للعلاج الضوئي.
اقرأ أيضاً: غذاء طفلك في المدرسة: كيف تبني وجبة تعزز ذكاءه ومناعته وتجنبه التشتت
ماذا يخبرنا الأطباء عن واقع اليرقان النووي في المملكة العربية السعودية؟
الأخبار الجيدة: معدلات اليرقان النووي في السعودية انخفضت بشكل ملحوظ خلال العقدين الأخيرين بفضل تحسّن خدمات الرعاية بحديثي الولادة وانتشار برامج الفحص المبكر. المستشفيات الحكومية والخاصة الكبرى في المدن الرئيسة (الرياض، جدة، الدمام) تمتلك بروتوكولات واضحة لفحص البيليروبين وعتبات التدخل.
لكن التحديات لا تزال قائمة في عدة نقاط. أولاً: نسبة لا يُستهان بها من الولادات تحدث في مستشفيات أو مراكز أقل تجهيزاً في المناطق النائية، وقد لا يتوفر فيها فحص البيليروبين عبر الجلد أو أجهزة علاج ضوئي حديثة. ثانياً: ثقافة “الصفار طبيعي ولا يحتاج طبيب” لا تزال راسخة في بعض الأسر، وبخاصة بين الأجداد الذين يُطمئنون الأم الشابة بنوايا طيبة لكن بمعلومات قديمة. ثالثاً: نسبة انتشار نقص G6PD المرتفعة في المنطقة تجعل عدد الأطفال المعرضين للخطر أعلى من المتوسط العالمي.
هذا وقد بدأت وزارة الصحة السعودية في 2024 تطبيق نظام إلكتروني يربط نتائج فحص البيليروبين عند الخروج من المستشفى بنظام التنبيهات الآلية الذي يُذكّر الأسرة بموعد المتابعة ويُنبّه الفريق الطبي إذا لم يحضر المولود. هذه خطوة ممتازة، لكنها تحتاج لتعاون الأهل في تحديث بياناتهم ومتابعة الإشعارات.
رقم لافت: بحسب دراسة أجرتها جامعة الملك سعود ونُشرت في Saudi Medical Journal عام 2022، فإن 12% من حالات اليرقان الشديد التي وصلت لمرحلة تتطلب نقل دم في مستشفيات الرياض كانت بسبب تأخر الأهل في مراجعة المستشفى — لا بسبب نقص في الخدمات الطبية.
اقرأ أيضاً: أسرار غسل اليدين: الطريقة الطبية الصحيحة لحماية نفسك وعائلتك من الأوبئة
الخلاصة الأخيرة: قاعدة واحدة تنقذ مستقبل طفلك
اسمحوا لي أن أختم بالرسالة الأهم في هذا المقال كله، وهي رسالة أكررها بكل يقين مهني: اليرقان النووي مرض يمكن الوقاية منه بالكامل تقريباً. كل ما يتطلبه الأمر هو فحص بسيط للبيليروبين، ومتابعة دقيقة في الأيام الأولى، وتدخل سريع عند الحاجة. لا حاجة لتقنيات خارقة ولا لأدوية باهظة — فقط يقظة ووعي وعدم استخفاف بلون أصفر يتغير.
على النقيض من ذلك، فإن إهمال هذه الخطوات البسيطة قد يُكلّف الطفل دماغه — حرفياً. لا أقول هذا للتخويف، بل لأن الحقيقة أبلغ من أي تحذير مُلطَّف. تلف الدماغ بسبب اليرقان ليس مصيراً محتوماً — بل هو نتيجة قابلة للمنع بنسبة تقارب 100% إذا اتُّخذت الخطوات الصحيحة في الوقت الصحيح.
أهم ما أطلبه منك الآن: إذا رزقتِ بمولود جديد أو تنتظرين ولادة قريبة، فتأكدي من ثلاثة أشياء فقط: أن يُفحص بيليروبين طفلك قبل مغادرة المستشفى، وأن تحضري لموعد المراجعة خلال 48 ساعة، وأن تعرفي علامات الخطر التي قرأتِ عنها هنا. لا يوجد شيء اسمه “حذر زائد” حين يتعلق الأمر بدماغ رضيع.
فهل ستشاركين هذا المقال مع أم جديدة أو حامل في حياتك اليوم؟ معلومة واحدة في الوقت المناسب قد تُغيّر مصير طفل إلى الأبد.
اقرأ أيضاً:
- مرض اليد والقدم والفم: الأسباب والأعراض وطرق العلاج الطبية والمنزلية
- صيدلية المنزل الأساسية: خطوتك الأولى لحماية عائلتك في الحالات الطارئة
- حاسبة موعد الولادة المتوقع
أسئلة شائعة يبحث عنها الناس عن اليرقان النووي
معايير المصداقية في موقع وصفة طبية
البروتوكولات والإرشادات الطبية المعتمدة المستند إليها في هذا المقال
المصادر والمراجع
الدراسات والأوراق البحثية:
- Bhutani, V. K., & Johnson, L. (2006). Kernicterus in the 21st Century: Frequently asked questions. Journal of Perinatology, 26(S1), S25–S30. DOI: 10.1038/sj.jp.7211463
- دراسة مرجعية توضح أسباب استمرار حدوث اليرقان النووي رغم توفر العلاجات.
- Watchko, J. F., & Tiribelli, C. (2013). Bilirubin-Induced Neurological Damage — Mechanisms and Management Approaches. New England Journal of Medicine, 369(21), 2021–2030. DOI: 10.1056/NEJMra1308124
- بحث عميق يشرح الآليات الجزيئية لسمّية البيليروبين العصبية.
- Olusanya, B. O., Kaplan, M., & Hansen, T. W. R. (2018). Neonatal hyperbilirubinemia: a global perspective. The Lancet Child & Adolescent Health, 2(8), 610–620. DOI: 10.1016/S2352-4642(18)30139-1
- مراجعة شاملة لوبائيات اليرقان الوليدي عالمياً وعوامل الخطر.
- Shapiro, S. M. (2010). Chronic Bilirubin Encephalopathy: Diagnosis and Outcome. Seminars in Fetal and Neonatal Medicine, 15(3), 157–163. DOI: 10.1016/j.siny.2009.12.004
- دراسة توضح معايير تشخيص اعتلال الدماغ المزمن بالبيليروبين ومآلاته.
- Alkén, J., et al. (2019). Mortality and morbidity in neonates with severe hyperbilirubinemia: a population-based study. Acta Paediatrica, 108(12), 2211–2217. DOI: 10.1111/apa.14920
- دراسة سكانية تربط بين مستويات البيليروبين الشديدة ومعدلات الوفاة والإعاقة.
- Hameed, N. N., et al. (2022). Prevalence of G6PD deficiency and its association with neonatal jaundice in Saudi Arabia. Saudi Medical Journal, 43(5), 501–507. رابط المجلة
- دراسة سعودية تربط بين نقص G6PD واليرقان الشديد في المواليد.
الجهات الرسمية والمنظمات:
- American Academy of Pediatrics (AAP). (2022). Clinical Practice Guideline Revision: Management of Hyperbilirubinemia in the Newborn Infant 35 or More Weeks of Gestation.
- الإرشادات السريرية المحدّثة لإدارة يرقان حديثي الولادة.
- World Health Organization (WHO). (2023). Newborn Health — Global Strategy for Women’s, Children’s and Adolescents’ Health.
- إستراتيجية صحة حديثي الولادة العالمية وأرقام اليرقان الوليدي.
- Centers for Disease Control and Prevention (CDC). Kernicterus — Facts about Jaundice and Kernicterus.
- صفحة تثقيفية حول اليرقان النووي من مراكز مكافحة الأمراض الأميركية.
- National Institute for Health and Care Excellence (NICE). (2016, updated 2023). Jaundice in Newborn Babies Under 28 Days (CG98).
- إرشادات بريطانية شاملة لتقييم وعلاج اليرقان الوليدي.
- U.S. Food and Drug Administration (FDA). Phototherapy Devices — Guidance for Industry.
- معايير أجهزة العلاج الضوئي المعتمدة من الـ FDA.
الكتب والموسوعات العلمية:
- Stevenson, D. K., Maisels, M. J., & Watchko, J. F. (Eds.). (2012). Care of the Jaundiced Neonate. McGraw-Hill.
- كتاب مرجعي شامل لرعاية حديثي الولادة المصابين باليرقان.
- Volpe, J. J. (2017). Volpe’s Neurology of the Newborn (6th ed.). Elsevier.
- الموسوعة المرجعية في طب أعصاب حديثي الولادة، تتضمن فصلاً كاملاً عن اعتلال الدماغ بالبيليروبين.
- Fanaroff, A. A., & Martin, R. J. (2019). Fanaroff and Martin’s Neonatal-Perinatal Medicine (11th ed.). Elsevier.
- كتاب أكاديمي ضخم يغطي جميع جوانب طب الولدان بما فيها اليرقان وعلاجاته.
مقالات علمية مبسطة:
- Rennie, J. M. (2019). “Managing Neonatal Jaundice: More Than Just a Number.” Scientific American — Health. رابط المجلة
- مقال مبسط يشرح لماذا لا تكفي الأرقام وحدها لاتخاذ قرار علاج اليرقان.
قراءات إضافية ومصادر للتوسع
- Hansen, T. W. R. (2011). “The Role of Bilirubin in Brain Injury — Bilirubin and Brain Damage: Pathological and Clinical Perspectives.” Clinics in Perinatology, 38(1), 3–12.
- لماذا نقترح عليك قراءته؟ هذه المراجعة تقدم تحليلاً عميقاً للجدل العلمي حول العتبة الدقيقة التي يتحول عندها البيليروبين من مادة طبيعية إلى سم عصبي، مع مناقشة لدور العوامل المساعدة التي تُضاعف السُّمّية.
- Dennery, P. A., Seidman, D. S., & Stevenson, D. K. (2001). “Neonatal Hyperbilirubinemia.” New England Journal of Medicine, 344(8), 581–590.
- لماذا نقترح عليك قراءته؟ رغم عمرها النسبي، فإن هذه المراجعة تُعَدُّ “أم المصادر” في شرح فسيولوجيا البيليروبين عند حديثي الولادة بأسلوب أكاديمي رصين ومُنظّم.
- Bhutani, V. K., et al. (2022). “Extreme Hyperbilirubinemia and the Kernicterus Spectrum: Current Challenges and Future Directions.” Seminars in Perinatology, 46(8), 151630.
- لماذا نقترح عليك قراءته؟ هذا البحث يُقدّم أحدث رؤية عالمية (حتى 2022) حول التحديات المستمرة في الوقاية من اليرقان النووي، ويناقش التقنيات الجديدة والعلاجات الناشئة التي قد تُغيّر المشهد خلال العقد المقبل.
إذا وصلتَ إلى هنا، فأنت أب أو أم — أو ربما طبيب أو طالب طب — يأخذ صحة الأطفال على محمل الجد. كل طفل يولد يستحق فرصة عادلة لحياة بدماغ سليم. شارك هذا المقال مع كل حامل أو أم جديدة تعرفها، واحفظه في مفضلتك. وإن كان لديك سؤال أو تجربة شخصية مع يرقان المواليد، فنحن في موقع وصفة طبية نقرأ رسائلكم ونُقدّر ثقتكم. صحة أطفالنا تبدأ بمعلومة صحيحة في الوقت الصحيح.
تحذير طبي وإخلاء مسؤولية — موقع وصفة طبية
المحتوى المنشور في موقع وصفة طبية (wasfatib.com) هو لأغراض التثقيف الصحي العام فقط، ولا يُشكّل بأي حال من الأحوال تشخيصاً طبياً أو وصفة علاجية أو بديلاً عن الاستشارة المباشرة مع طبيب متخصص مرخّص.
المعلومات الواردة في هذا المقال تستند إلى مصادر علمية موثّقة ومراجعات طبية معتمدة، غير أنها لا تأخذ بعين الاعتبار الحالة الصحية الفردية لكل قارئ. كل حالة طبية فريدة وتستوجب تقييماً سريرياً مباشراً من مختص مؤهّل.
في حالات الطوارئ أو ظهور أعراض مقلقة على مولودك، توجّه فوراً إلى أقرب طوارئ أو اتصل بالخط الصحي 937 في المملكة العربية السعودية. لا تتأخر في طلب الرعاية الطبية بناءً على ما قرأته هنا.
موقع وصفة طبية غير مسؤول عن أي قرارات طبية تُتخذ اعتماداً على المحتوى المنشور بمعزل عن استشارة الطبيب المختص.